US Pharm. 2008;33(3)(OTC suppl):4-7.
Az asztma egy olyan tüdőbetegség, amelyet reverzibilis légáramlási obstrukció és hörgő túlreagálás jellemez. Az asztma központi jellemzője a gyulladás, amely visszatérő epizódokhoz, ziháláshoz, köhögéshez, légszomjhoz és mellkasi szorító érzéshez vezet.1,2 A terápia célja a betegség kontrolljának elérése a normális életminőség fenntartása érdekében.
Az asztma terhe az elmúlt három évtizedben folyamatosan nőtt. Az 1970-es években a lakosság körülbelül 3%-a szenvedett asztmában, míg 1995-ben 5,5%, illetve 2005-ben 7,7%.3 Ez utóbbi becslés körülbelül 22,2 millió amerikait jelent.2,3 A betegség gyakoriságának növekedésével az Egyesült Államokban az asztma miatti morbiditás és mortalitás is növekszik. 2004-ben az asztmának tulajdonítható 1,8 millió sürgősségi osztályon tett látogatás, 497 000 kórházi kezelés és 4055 haláleset volt.3
Az asztma kontrollján alapuló kezelés
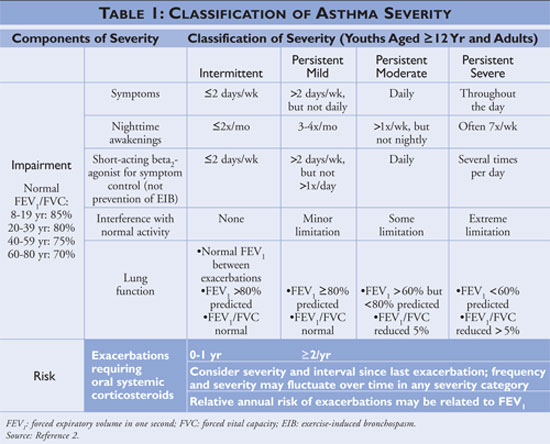
A National Asthma Education and Prevention Program (NAEPP), a National Heart, Lung, and Blood Institute részlege, az asztma diagnózisára és kezelésére vonatkozó irányelveket tesz közzé, amelyeket legutóbb 2007-ben frissítettek.2 Az irányelvek a tünetek és a gyorsan ható gyógyszerek használatának gyakorisága alapján az asztma súlyosságát időszakos vagy tartósnak minősítik. Az időszakos asztmás egyéneknél a tünetek ritkán jelentkeznek, következésképpen ritkán használnak gyorsan ható gyógyszereket, és nem zavarják a normál tevékenységet. Ha az asztma kevésbé kontrollált, akkor az asztma súlyossága a tartósnak minősül (lásd az 1. TÁBLÁZATOT).
Az irányelvek az asztma kezelésének sarokköveiként az önkezelési oktatást, a gyorsan enyhülő gyógyszerek alkalmazását és a tartósan fennálló asztmában szenvedő egyéneknél a tartósan kontrollált gyógyszerek alkalmazását írják le. Az önkezelési oktatást nyújtó egészségügyi szolgáltatóknak utasítaniuk kell a betegeket az asztmát kiváltó okok azonosítására és lehetőség szerinti elkerülésére, a farmakológiai terápiák megfelelő alkalmazására, valamint az asztma cselekvési terv kidolgozására. A gyors hatású gyógyszeres kezelést minden asztmás betegnél el kell kezdeni, és az időszakos asztmában szenvedő egyéneknél monoterápiaként is alkalmazható; a tartósan fennálló asztmával diagnosztizált egyéneknél azonban egy vagy több hosszú távú ellenőrző gyógyszerrel kell kiegészíteni a kezelést. A hosszú távú ellenőrző gyógyszerek közé tartoznak az inhalációs kortikoszteroidok, a leukotriénmódosítók, a hosszú hatású béta-agonisták és a teofillin (lásd a 2. TÁBLÁZATOT).

Az irányelvek azt is megjegyzik, hogy az amerikai lakosság mintegy 30%-a használ kiegészítő és alternatív gyógyszereket és beavatkozásokat. Jelenleg azonban nem áll rendelkezésre elegendő bizonyíték ahhoz, hogy ezeket a kezelési módokat az asztma kezelésére ajánlják. Az irányelvek a biztonsági és hatékonysági adatok hiánya miatt nem javasolják a gyógynövényes szerek alkalmazását az asztma kezelésére.
A vény nélkül kapható asztmakészítmények és szabályozásuk
A vény nélkül kapható asztmakészítmények az 1950-es évek óta kaphatók, bár egyes hatóanyagok az évek során jelentősen megváltoztak. A jelenleg kapható vény nélkül kapható hatóanyagok az efedrin – guaifenezinnel vagy anélkül – és az adrenalin. A teofillin és a fenobarbitál korábban a vény nélkül kapható asztmakészítmények hatóanyagai voltak; azonban ma már mindkettő a vényköteles készítmények közé tartozik.4
Az elmúlt három évtizedben az FDA intézkedéseket hozott az asztma vény nélkül kapható kezeléseinek szabályozására vonatkozóan. Az FDA 1976-ban arra a következtetésre jutott, hogy az inhalált adrenalin gyors és hatékony enyhülést biztosít enyhe és közepesen súlyos asztma esetén. 1982-ben egy előzetes végleges monográfiában ismét arra a következtetésre jutott: “Az epinefrin, az epinefrin-bitartarát és az epinefrin-hidroklorid (racém; azóta átnevezték razepinefrin-hidrokloridra) nyomás alatt álló, adagolt inhalációs aeroszol adagolóformákban általánosan biztonságosnak és hatékonynak ismerhető el vény nélkül kapható felhasználásra, felnőttek és 4 éves és idősebb gyermekek esetében 1-2 inhalációnyi adagolt dózisban, ami megfelel 0,0-nak.16-0,25 mg epinefrin inhalációnként, legfeljebb 3 óránként. “5,6
1986-ban az FDA felülvizsgálta a hörgőtágító efedrintermékeket, és engedélyezte, hogy ez a hatóanyag vény nélküli használatra általánosan biztonságosnak és hatékonynak minősüljön. Abban az évben az FDA úgy döntött, hogy az adatok nem elegendőek ahhoz, hogy az inhalációs epinefrint csak vényköteles használatra korlátozzák, és hogy a vény nélküli hozzáférhetőség előnyei meghaladják a kockázatokat. Az FDA arra a következtetésre jutott, hogy a kiterjesztett és felülvizsgált címkézés előnyös lenne a fogyasztók számára.5,6
A teofillint tartalmazó, vény nélkül kapható kombinált termékeknek tulajdonítható életveszélyes eseményekről és halálesetekről szóló jelentések után az FDA 1995-ben végleges határozatot hozott arról, hogy ezek a termékek nem biztonságosak és nem hatékonyak.7 Így az efedrin és teofillin kombinációját tartalmazó termékeket megszüntették, néhányat pedig úgy alakítottak át, hogy efedrin és guaifenezin tartalmú legyen. Szintén 1995-ben az FDA javasolta az efedrin vény nélkül kapható termékek piacról való kivonását a metamfetamin és a metkatinon előállításában játszott szerepe, valamint a súlykontrollra és izomnövelésre való visszaélése miatt.7
1996-ban az FDA módosította az 1986-os végleges monográfiát, hogy megszüntesse az OTC hörgőtágítók monográfiai státuszát.6 Ehelyett minden új, vény nélkül kapható adagolós inhalátor gyártójának jóváhagyott kérelmet kell benyújtania, amely a monográfiában nem szereplő információkat tartalmaz.6 A jelenleg forgalomban lévő, vény nélkül kapható hörgőtágítókra ez a módosítás nem volt hatással.
Az FDA azon javaslata ellenére, hogy az efedrin a metamfetamin előállításában alapelemként való felhasználása miatt kerüljön ki a vény nélkül kapható termékek piacáról, a termék továbbra is vény nélkül kapható. Ehelyett a 2005-ös Combat Methamphetamine Epidemic Act of 2005, amely 2006-ban beépült a Patriot Act-be, az efedrin-tartalmú, vény nélkül kapható termékeknek vény nélkül kapható státuszt biztosított.8 Az efedrint tartalmazó termékeket vásárolni kívánó fogyasztóknak mostantól a gyógyszertárban be kell mutatniuk a kormány által kiállított fényképes igazolványt, mivel ezeket a termékeket már nem árusítják legálisan a regisztrált gyógyszertár nélküli kisboltokban vagy raktárüzletekben.
A globális közegészségügy védelmének részeként nemzetközi megállapodás jött létre az ózonlebontó anyagokat (ODS) tartalmazó termékek, például az adagolós inhalátorokban található fluorozott-klórozott szénhidrogének (CFC) csökkentésére és végül megszüntetésére. Ez a megállapodás vezetett az 1987-es Montreali Jegyzőkönyvhöz, majd az 1990-es Tiszta Levegő Törvény módosításaihoz.9-11 A megállapodás mentességet biztosít a CFC-k használata alól az asztma kezelésére használt MDI-kben, ha a termék használatát az FDA alapvető fontosságúnak minősíti.12 A nem vényköteles asztmagyógyszerek továbbra is az alapvető fontosságúnak minősített felhasználás alatt maradtak. Az FDA azonban 2007-ben bejelentette, hogy javaslatot tesz az inhalációs adrenalin alapvető felhasználásra való kijelölésének 2010. december 31-i hatállyal történő megszüntetésére.13 Az FDA az alábbi, a 21 CFR 2.125(g)(2) bekezdésében található kritériumokat használta az inhalációs adrenalin alapvető felhasználásra való kijelölésének felülvizsgálatához: “(i): Jelentős technikai akadályok állnak fenn a termék ODS-ek nélküli előállítása előtt; (ii): A termék elérhetetlenül fontos közegészségügyi előnyt biztosít; és (iii): A termék használata nem bocsát ki halmozottan jelentős mennyiségű ODS-t a légkörbe, vagy a kibocsátás indokolt, tekintettel a nem elérhető fontos közegészségügyi előnyre. “13 Az FDA jelenleg várja az észrevételeket ebben a kérdésben, mielőtt végleges döntést hozna.
A vény nélkül kapható termékek biztonságossága és hatékonysága
Amint azt az FDA által az asztmás termékek vény nélkül kapható státuszával kapcsolatban tett különböző javaslatok és intézkedések is bizonyítják, az elmúlt évtizedekben sok vita folyt az e termékekben lévő hatóanyagok biztonságosságáról és hatékonyságáról. Bár ezeket a termékeket nem reklámozzák aktívan, elérhetőségük azt jelenti, hogy biztonságuk és hatékonyságuk kritikusan fontos a fogyasztók számára.
Ephedrin: Az egy összetevőből álló, hörgőtágítóként használt efedrin termékeket az FDA 1986 óta általánosan biztonságosnak és hatékonynak tekinti.14 Az efedrin epinefrint szabadít fel a szövetekből, amely alfa-adrenerg és nem szelektív béta-adrenerg receptor aktivitást vált ki. Az efedrin hörgőtágító hatékonyságát az 1950-es évektől kezdődően végzett vizsgálatok bizonyították. Az efedrin hörgőtágítóként kevésbé kívánatos tulajdonságai közé tartozik az inhalációs készítményeknél lassabb hatáskezdet (15 perctől egy óráig) és a béta-stimuláció nem szelektivitása, ami hozzájárulhat a kardiovaszkuláris mellékhatásokhoz (AE).15-17 A vizsgálatok azonban ellentmondásos eredményeket mutattak az efedrin 12,5-25 mg-os címkézett dózisban történő alkalmazásának tulajdonítható kardiovaszkuláris mellékhatások tekintetében.16
Epinefrin: Az adrenalin ugyanolyan alfa- és béta-adrenerg receptor aktivitást mutat, mint az efedrin; ezért ugyanazok az aggályok merülnek fel a kardiovaszkuláris AE-k lehetőségével kapcsolatban. Az inhalációs epinefrin hatásának kezdete (15 másodperc) sokkal gyorsabb, mint az orális efedriné, így megfelelőbb választás akut asztmás exacerbáció azonnali enyhítésére.6 Rövid hatástartama (23 perc) azonban szükségessé teheti, hogy a beteg a folyamatos enyhítés érdekében ismételten használja a készítményt, ahelyett, hogy követné a címkén szereplő, három órán belül legfeljebb két inhalációra vonatkozó utasítást.6 6 A vény nélkül kapható adrenalin-inhalátorok biztonságosnak és hatékonynak tűnnek az enyhe, időszakos asztmás betegek számára, ha a címkén feltüntetett módon használják őket.5 Ez azonban továbbra is viták forrása, mivel sok egészségügyi szolgáltató aggódik amiatt, hogy a vény nélkül kapható inhalátorokra hagyatkozó betegek esetleg nem kapnak megfelelő betegségkezelést az egészségügyi csapattól, ami súlyos következményekkel járhat.
Guaifenesin: A guaifenesint efedrinnel kombinációban használják asztma kezelésére, és biztonságosnak és hatékonynak ismerik el, ha a készítményt asztmával összefüggő köhögés kezelésére jelölik.14 Bár a guaifenesin az FDA által jóváhagyott nyákoldószer, hörgőtágító hatással nem rendelkezik. Így nem járul hozzá további előnyökkel az efedrin termékhez akut súlyosbodás esetén.17
A vény nélkül kapható asztmakészítmények használata
A Wyeth Consumer Healthcare (WCH) 1999-ben végzett felmérése szerint nagyjából hatmillió (30%) asztmás személy használ epinefrin inhalálót.6 A válaszadók önbevallása szerint e hatmillió embernek körülbelül 20%-a sorolható enyhe vagy közepesen súlyos, tartós asztmások közé, ami nem tartozik a termék címkén feltüntetett felhasználási területéhez.5 A NAEPP irányelvei a rövid hatású béta-agonisták legalább szükség szerinti használatát szorgalmazzák minden asztmában szenvedő egyénnél; az irányelvek azonban nem említik kifejezetten az inhalált adrenalint, mint kezelési lehetőséget.
2005-ben a WCH 330 személy körében végzett internetes felmérést a vény nélkül kapható hörgőtágítóknak a tüneteik kezelésére történő alkalmazásáról. A WCH megállapította, hogy a nem vényköteles hörgőtágítót használók 92%-ánál diagnosztizáltak asztmát, 91%-uk csak akut asztmás súlyosbodás esetén használt inhalált adrenalint, 31%-uknak nem volt egészségbiztosítása, és 38%-uknak nem volt vényköteles biztosítása.6 A WCH ezeket az eredményeket extrapolálva úgy becsülte, hogy az asztmás egyének körülbelül 5-10%-a használ monoterápiaként nem vényköteles hörgőtágítókat.6 A vény nélkül kapható készítmények használatának elsődleges okai – a könnyű hozzáférés és az alacsonyabb költségek – közvetlenül összefüggnek az egészségügyi szolgáltatók azon aggodalmaival, hogy a vény nélkül kapható asztmás készítményeket használó személyek esetleg nem részesülnek megfelelő betegségkezelésben.6
Diszkusszió
Az akut asztma kezelésében kívánatos tulajdonságok közé tartozik a hörgőtágító hatékonyság, a biztonságosság a címkén feltüntetett módon történő alkalmazás esetén, a gyors hatáskezdet és a hosszú hatástartam. Mind az inhalációs epinefrin, mind az orális efedrin évtizedek óta bizonyítja hatékonyságát a vizsgálatokban. Tekintettel azonban a klinikai vizsgálatok vegyes kardiovaszkuláris eredményeire, a vény nélkül kapható hörgőtágítók olyan egyének általi használatának biztonságossága, akiket esetleg nem követnek orvosilag, komoly aggodalomra ad okot az egészségügyi szolgáltatók számára. Az inhalált epinefrin gyorsabban kezd hatni, mint a szájon át szedett efedrin, de rövid hatástartama korlátozhatja hatékonyságát.
A szájon át szedett efedrin elérhetőségét 2006 óta korlátozza a vény nélkül kapható státusz. Az inhalálható epinefrin hozzáférhetősége az FDA döntésétől függ, hogy ez a készítmény fenntartja-e az alapvető felhasználásra való kijelölést. A jelenleg forgalmazott, CFC-tartalmú, vény nélkül kapható hörgőtágítóknak nincs vény nélkül kapható alternatívája.12 Az egyik gyártó megpróbálta vény nélkül kapható inhalációs adrenalin termékét hidrofluoralkán hajtógázzal újrafogalmazni, ami a felhasználó számára nemkívánatos hatásokkal járt; a gyártó egy másik gyógyszeripari céggel társult az újrafogalmazás érdekében, és arra számít, hogy 2011-re benyújtja a kérelmet az FDA-hoz.6 Az alternatív hajtógázzal kapcsolatos fő aggályok közé tartozik az adrenalin hatékony adagolásának szükségessége, valamint az új termékre vonatkozó biztonsági és hatékonysági adatok a változások eredményeként.18
Az FDA nem a jelenleg forgalmazott, CFC-tartalmú termékek biztonságosságát vagy hatékonyságát vizsgálja annak eldöntése során, hogy az inhalálható adrenalinra vonatkozó alapvető felhasználási jelölést visszavonják-e. Inkább azt vizsgálja, hogy a jelölés visszavonása milyen hatással lenne a közegészségügyre. A National Association of Chain Drug Stores és az American Pharmacists Association által az FDA-nak írt levelekben, amelyekben az alapvető felhasználásra vonatkozó jelölés megszüntetésére vonatkozó javaslattal kapcsolatban az elsődleges aggodalom a vény nélkül kapható inhalátorok jelenlegi felhasználóira gyakorolt lehetséges negatív hatás volt, ha a termékek nem lennének elérhetők.19,20 Az FDA kijelentette, hogy ha az alapvető felhasználásra vonatkozó jelölés megszüntetésére vonatkozó javasolt szabály végleges lesz, és nem léteznek vény nélküli alternatívák, a fogyasztóknak receptre kell majd kiváltaniuk egy alternatív terméket.12 Az inhalációs adrenalint használó fogyasztók közül sokan dönthetnek úgy, hogy lemondanak az asztma kezeléséről, vagy alternatív, nem vényköteles terápiát keresnek.
Elkerülhetetlen, hogy az orvostársadalom felhívja a közvélemény figyelmét a kontrollálatlan asztma következményeinek súlyosságára, és hogy minden olyan személy, aki légzési nehézségeket tapasztal, keressen fel egy egészségügyi szolgáltatót diagnózis és kezelés céljából. A vény nélkül kapható hörgőtágítók használata mellett döntő betegnek azt kell tanácsolni, hogy tájékoztassa erről egészségügyi szolgáltatóját; a betegnek tanácsot kell adni a vény nélkül kapható és a vényköteles inhalátorok címkén szereplő utasítások közötti különbségről is. A vény nélkül kapható hörgőtágítók jelenlegi folyamatos hozzáférhetősége szükségessé teszi a betegek tájékozott tanácsadását e termékek helytelen használatának és a későbbi káros hatásoknak a megelőzése érdekében.
1. Moorman JE, Rudd RS, Johnson CA, et al. National Surveillance for Asthma–United States, 1980-2004. MMWR. Oct 19, 2007;56:1-14, 18-54.
2. Szakértői testület jelentése 3: Az asztma diagnózisára és kezelésére vonatkozó iránymutatások. Nemzeti Asztma Oktatási és Megelőzési Program. Bethesda, MD: National Heart, Lung, and Blood Institute, National Institutes of Health; 2007.
3. Akinbami L. Asthma prevalence, health care use and mortality: Egyesült Államok, 2003-05. National Center for Health Statistics. www.cdc.gov/nchs/products/pubs
/pubd/hestats/ashtma03-05/asthma03-05.htm. Hozzáférés 2007. december 10.
4. W. Steven Pray. OTCtermékek és az asztma terápia. US Pharm. 1997;22(7):18-22.
5. Dickinson BD, Altman RD, Deitchman SD, Champion HC. A vény nélkül kapható asztmás inhalátorok biztonságossága: a Tudományos Ügyek Tanácsának jelentése. Chest. 2000;118:522-526.
6. Wyeth ConsumerHealthcare. 2005N-0374. Ózonlebontó anyag használata: a vény nélkül kapható adrenalin-adagoló inhalátorok alapvető használatának meghatározása. Tájékoztató dokumentum. December 19, 2005. www.fda.gov/ohrms/dockets/ac
/06/briefing/2006-4200B1_01_01-Wyeth-Backgrounder.pdf. Hozzáférés 2007. december 30.
7. Kupec IF. Teofillin tartalmú hörgőtágítók és efedrin hatóanyagú gyógyszerek. Válaszok T95-40. 1995. július 27. www.fda.gov/bbs/topics/ANSWERS/ANS00675.html. Hozzáférés 2007. december 10.
8. Drug Enforcement Administration. Általános információk a 2005. évi, a metamfetamin-járvány elleni küzdelemről szóló törvényről . 2006. május. www.deadiversion.usdoj.gov/meth/cma2005_general_info.pdf. Hozzáférés 2008. február 4.
9. Jarabek AM, Fisher JW, Rubenstein R, et al. Mechanistic insights help the search for CFC substitutes: risk assessment of HCFC-123 as an example. Risk Anal. 1994;14:231-250.
10. DeCanio SJ, Norman CS. A Montreali Jegyzőkönyv szerinti, az adagolós inhalátorokra vonatkozó “alapvető felhasználási mentességek” gazdaságossága. J Environ Manage.2007;85:1-8.
11. D’Souza S. A Montreali Jegyzőkönyv és az alapvető felhasználásra vonatkozó mentességek. J Aerosol Med. 1995;8(suppl 1):S13-S17.
12. Food and Drug Administration (Élelmiszer- és Gyógyszerügyi Hivatal). FDA News. Az FDA javasolja a CFC-k fokozatos kivonását az epinefrin adagoló inhalátorokból. www.fda.gov/bbs/topics/NEWS
/2007/NEW01706.html. Hozzáférés 2007. december 10.
13. Food and Drug Administration (Élelmiszer- és Gyógyszerügyi Hivatal). Code of Federal Regulation 21 CFR 2. rész 2007N-0262. www.fda.gov/ohrms/dockets/98fr/cd0612.pdf. Hozzáférés 2008. február 6.
14. Whitehall-Robins. RE: docket no. 98N-0148; Fed. Reg. 13258, nemzetközi kábítószer-listázás; Egyezmény a pszichotróp anyagokról. 1998. április 16. www.fda.gov/ohrms/dockets/dockets/98n0148/c000010.pdf. Hozzáférés 2007. december 30.
15. Lexi-Comp Online. www.crlonline.com. Hozzáférés 2007. december 28.
16. Tashkin DP, Meth R, Simmons DH, Lee YE. Az orális terbutalin és efedrin akut bronchiális és kardiovaszkuláris hatásainak kettős vak összehasonlítása. Chest. 1975;68:155-161.
17. Dulfano MJ. Az új orális hörgőtágítók . Chest.1975;68:133-134.
18. Megfázás, köhögés, allergia, hörgőtágító és asztmaellenes gyógyszerek vény nélkül kapható emberi felhasználásra; az OTC hörgőtágító gyógyszerek monográfiájának módosítása. Fed Regist. 1996; 61:25142-25147.
19. National Association of Chain Drug Stores (Gyógyszertárláncok Országos Szövetsége). Tárgy: Ózonlebontó hajtógázok használata; a vény nélkül kapható epinefrin adagolós inhalátorok (MDI-k) alapvető felhasználási jelölésének visszavonása. január 6. www.fda.gov/ohrms/dockets/dockets/05n0374/05n-0374-EC6-Attach-1.pdf. Hozzáférés 2008. február 6.
20. Az Amerikai Gyógyszerészek Szövetségének (APhA) nyilatkozata az Élelmiszer- és Gyógyszerügyi Hivatal vény nélkül kapható gyógyszerek tanácsadó bizottságának és a tüdő-allergiás gyógyszerek tanácsadó bizottságának. Ózonlebontó anyag használata: az OTC epinefrin adagolós inhalátorok alapvető felhasználásának meghatározása. január 24. 2006. www.fda.gov/ohrms/dockets/dockets/05n0374/05N-0374-EC10-Attach-1.pdf. Hozzáférés 2008. február 6.
A cikkel kapcsolatos észrevételekért forduljon a [email protected] címre.