
A citromlé íze savanyú, mert 5-6% citromsavat tartalmaz, és pH-ja 2,2-es. (magas savasság)
A pH (hidrogénpotenciál) egy 0-tól 14-ig terjedő savassági skála. Megmutatja, hogy egy anyag mennyire savas vagy lúgos. A savasabb oldatok, alacsonyabb pH-val rendelkeznek. Lúgosabb oldatok, magasabb pH-val rendelkeznek. A nem savas vagy lúgos anyagok (azaz a semleges oldatok) pH-ja általában 7. A savak pH-ja 7-nél kisebb. A lúgok pH-ja 7-nél nagyobb.
A pH az oldatban lévő protonok (H+) koncentrációjának mértékegysége. S.P.L. Sørensen 1909-ben vezette be ezt a fogalmat. A p a német potenz, azaz erő vagy koncentráció, a H pedig a hidrogéniont (H+) jelenti.
A lúgos anyagok hidrogénionok helyett hidroxidionok (OH-) koncentrációjával rendelkeznek.
pH indikátorok
A pH indikátor olyan kémiai vegyület, amelyet kis mennyiségben adnak egy oldathoz, így láthatóvá válik az oldat pH-ja (savassága vagy lúgossága). A pH-indikátor a hidróniumionok (H3O+) vagy hidrogénionok (H+) kémiai detektora. Általában az indikátor hatására az oldat színe a pH függvényében változik.
A tipikus indikátorok a fenolftalein, a metilnarancs, a metilvörös, a brómtimol-kék és a timol-kék. Ezek mindegyike a pH-skála különböző pontjain változtatja a színét, és együttesen univerzális indikátorként használhatók.
Egy másik lehetőség a lakmuszpapír használata, amely egy természetes pH-indikátoron alapul. A papír meg tudja mondani, hogy a vegyszer milyen erős, erősebb sav vagy erősebb bázis.
Néhány gyakori pH-érték
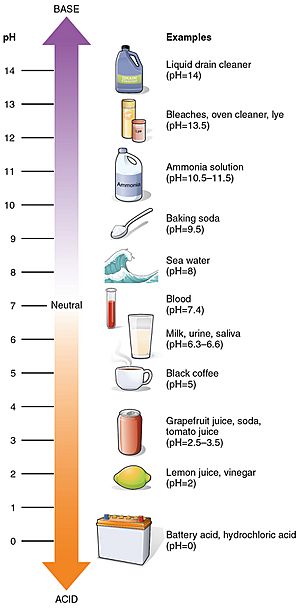
Néhány gyakori anyag pH-értéke
Semlegesítés
A semlegesítés az egyenlet segítségével összegezhető:
H+ + OH- → H2O
(sav + bázis → víz)
Kapcsolódó oldalak
- Sav
- Bázis
- Lúg
- Titrálás
- Transzpiráció(Sreekanta Das).
Képek gyerekeknek
-
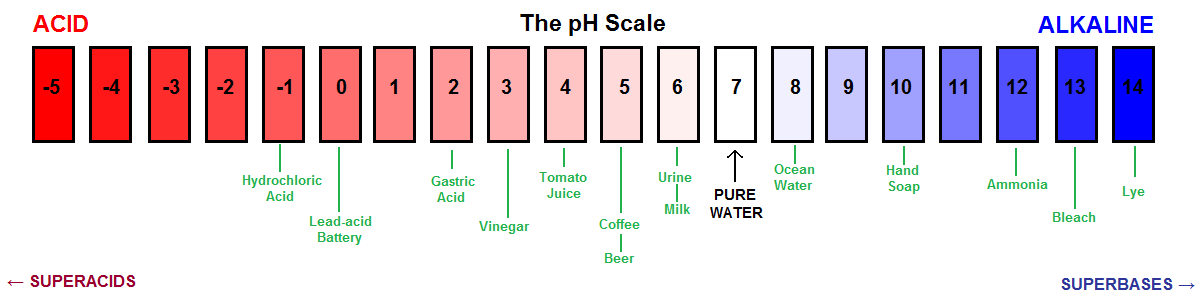
A pH-skála másik vizuális ábrázolása.
-

A vérvizsgálatok referenciatartományai, balra a protonok koncentrációja (lila). Látható, hogy a tartományokat szűk tartományban tartják, és hogy a szabad protonok a legkisebb tömegkoncentrációjú vegyületek közé tartoznak.
-

Az univerzális indikátorpapír színének a pH-val való változását bemutató grafikon