ほとんどの化学者は、自分の人生を形作った論文を挙げることができる。 私たちの多くにとって、最も関連性の高いものの1つが、1966年のCahn-Ingold-Prelog(CIP)優先順位規則である。 この論文は印象的な引用数を誇っていますが、それと同じくらい重要なのは、その人気の安定性です。その実用的な有用性により、世界中の化学者の世代で使われ続けているのです。
共有化学結合は CIP 規則の基礎と見なされることが多いですが、超分子化学に不可欠な非共有結合の相互作用も立体中心を生じさせます。 2004 年、国際純正・応用化学連合 (Iupac) は、電子のペアを持つ四面体系の扱いに関して、「窒素や硫黄などの原子上の電子の単独ペアは、ゼロという架空の原子番号を持つ」と統合し、既存のルールにローンペアが含まれていることを明らかにしました。 窒素や硫黄のような原子上の孤立電子は、架空の原子番号0を持ち、水素原子より下位に位置する」。 そこで、非共有結合相互作用の問題を解決するために、優先順位のルールをさらに簡単に拡張することを提案します。
提案システム
ローンペアを含む相互作用について、配位ローンペアに 0 から 1 の架空の原子番号(言い換えれば非配位ローンペアより大きく、水素原子より小さい)が割り当てられることを提案します。 複数の配位子対がある場合、それらは古典的なCIP規則に従って配位子によって並べられる。
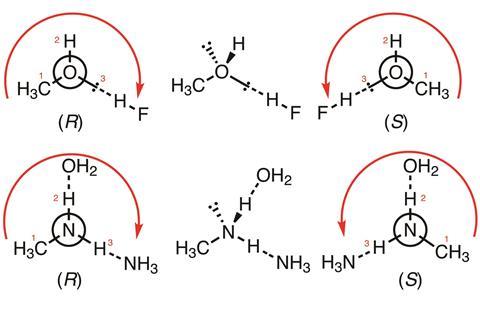
上の例は、CIP 規則への修正案を使用して、優先度がどのように与えられるか(赤い線と数字に従って)示しています
原子が関与する相互作用(たとえば水素結合の一部として H 原子)については、立体中心への適用と同じ規則によって割り当てが達成されるのです。 したがって、水素結合または他の非共有結合の相互作用は水素よりも優先度が高く、非共有結合はリガンドの原子番号で優先されます(最高から最低)。
上に2つの簡単な例を示しますが、優先順位を示すために矢印と数字が付けられています。 最初の例 (CH3OH:HF 錯体) では、メタノールに配位するローンペアは、非配位ローンペア (後ろ向き) と水素原子の間の中間の優先度を持ちます。2番目の例 (CH3NH2:NH3:OH2 錯体) は、酸素に配位する水素が、窒素に配位する水素より優先度が高くなります。 どちらもローンペア(後ろ向き)よりは優先度が高いが、メチル基よりは優先度が低い。
化合物を正しく命名することは、立体異性中心ができたことを自覚し、キラリティの起源について自問することであり、さらに、第2の超分子立体異性中心の存在により、隠れたジアステレオメリズムが生じることになる。 この単純なシステムによって、超分子構造を明確に記述することができ、化学の言語をさらに向上させることができる
。