大腸がんスクリーニングのための大腸内視鏡は、早期発見による死亡率低下と前がん性ポリーの除去による予防効果の双方がある (1-8). しかし、これらの利点は、大腸内視鏡検査の質の不備や合併症により相殺される可能性がある(9-17)。 見逃されたポリープや不完全なポリペクトミーは、interval cancer development (大腸内視鏡検査後に発見された癌) の一因となる可能性がある (10-14, 18, 19)。 大腸内視鏡検査後の出血は 1-6/1000 人と比較的まれであるが(15-17)、大腸内視鏡検査後 7 日以内に予定外の入院をする主要な合併症である (20)。 ポリペクトミーが圧倒的な原因である(21-26)。 ポリペクトミー後の出血を増加させる危険因子としては、ポリープの大きさ、ポリープの数、抗凝固療法、ポリープの組織学などが挙げられる(17, 21, 27, 28)。 内視鏡的粘膜切除術(EMR)や内視鏡的粘膜下層剥離術(ESD)などの高度なポリペクトミー技術は、より完全にポリープを除去できるようだが、手術時間、費用、出血リスクも増加する(17、29~31)。 実際、一般に広く受け入れられている従来のスネアポリペクトミー法は、熱凝固を伴うかどうかにかかわらず、固定されたポリープをギロチンで切断するもので、ほぼ50年間あまり変わっていない(32~37)。 大腸内視鏡検査で最も多く見られる非癌性ポリープは粘膜に限局しており、粘膜下層に進展していないため、ポリープ切除後の出血を防ぐために、著者(ZJC)の一人は従来のコールドスネアポリペクトミー(TCSP)の改良版として内視鏡的粘膜ストリップ(EMS)を開発し、血管に富む粘膜下層への切込みを避けた。 EMSは、粘膜下層に大きな損傷を与えることなく、非根拠性ポリープの完全切除に早期に成功したことから、2012年12月31日にこの技術革新をシステムとして採用することが決定された。 本報告では、特に高リスクの進行性ポリープに対して、ポリペクトミー後の出血を防ぎ、ポリープの完全切除を容易にするEMSの有効性について分析する。
方法
患者および研究デザイン
これはMinnesota Gastroenterology, PA(MNGI)の電子医療記録と病理スライドを組み込んだデータをもとに、後ろ向き調査を行ったものです。 内部審査委員会の免責を得た。 患者は,EMS時代以前(2005~2012年)とEMS時代(2013~2016年)の12年間に,MNGI外来内視鏡センターでZJCによるCurrent Procedural Terminology(CPT)コード45385のスネアポリペクトミー付き大腸内視鏡を受けた患者であった。 入院を要するポリープ切除後の出血症例と,絨毛の特徴を有するポリープ,高悪性度異形成,細胞学的異形成を有する無節鋸歯状腺腫(SSACD)および10 mm以上のあらゆる腺腫性ポリープと定義される進行性ポリープについてデータベース検索が行われた。 MNGIは地域の診療所を広くカバーし、24時間体制で合併症の電話相談を行っていたため、合併症の把握はほぼ完璧で、その内容はピアレビューされ、品質向上のために関係する内視鏡医にフィードバックされた。 これはTCSPを改良したもので,もともとTCSPで説明されていたように固定された組織全体をギロチンで切るのではなく,EMSは固定された粘膜下層の間にある粘膜を剥ぎ取る(図1,補足動画)ものである(36,37)。 したがって、EMSは粘膜下層の損傷とそれに伴う即時および遅発性出血を最小限に抑えることが期待される。 まれに発生するPedunculated Polypに対しては、焼灼による組織損傷は管内茎部に限定され、大腸壁の深部には及ばないため、現在でもホットスネアポリペクトミーを用いている。 そのため、EMSは悪性腫瘍を示唆する特徴を持たない非ペダンキュレーションポリープにのみ適用している。 以下では、ポリープサイズに応じたEMSの具体的な手法について詳述する。 EMSと従来のスネアポリペクトミーとの決定的な違いを説明する図。 Chen and Batts(38)、Copyright(2017)からエルゼビア社の許可を得て、CC-BYユーザーライセンスの下でオープンアクセスコンテンツとして使用するために転載
小さなポリープ(≤5mm)には、一般的にTCSPはよく機能します。 2mm以下の小さなポリープを除いては、完全切除のために生検鉗子よりもスネアを優先し(25)、ポリープ切除時に隣接粘膜を2~3mm切除することが日常的である。 しかし、粘膜下層がスネアの内側に入り込み、ギロチンや熱凝固法(ホットスネア)を用いないとスネアを完全に閉鎖することができないことがある。 このような場合、スネアをしっかりと閉じたままスコープ内に静かに挿入すると、通常、ポリープを含む粘膜が剥離/ピンセットされ、巻き込まれた粘膜下層が一過性に隆起した仮骨を形成します(図2A)。 内視鏡的には、剥離した粘膜は通常一枚であるが、粘膜下層は血管を傷つけずほぼ無傷のままである(図2B)。 EMSによる粘膜裂傷は、一般にTCSPによるものよりわずかに大きいが、血の気の少ないポリペクトミー部位を形成する。 EMSを効果的に行うには、ストリッピングの際にスネアをしっかりと閉じておくことが重要であるが、あまり強く閉じないこと。 スネアをしっかり閉めないとスネアスリップの原因となり、スネアを強く閉めすぎると血腫形成などの粘膜下障害やストリッピング失敗の原因となる。 経験豊富な内視鏡医であれば、その微妙な違いを容易に察知し、内視鏡看護師にスネアを引く際の適切な握り加減を指示することができる
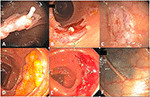
Figure 2. EMSポリペクトミー。 (A)10mm無茎性盲腸管状腺腫のポリペクトミー後の粘膜下仮骨。 (B)切除後のポリープを含む無傷の粘膜片(右上)と仮骨が確認できるポリープのないポリペクトミー部位(左下)。 (C)ポリープ切除直後の軽微な一過性の毛細血管滲出にもかかわらず、変形のないきれいなポリープ切除部位。 巻き込まれた粘膜を持ち上げることで、仮骨の発生を防ぐことができた。 (D)30mm横行結腸の無節性鋸歯状腺腫。 (E) (D)の断片的ポリペクトミー後のポリペクトミー部位。 (F) 1年後の(E)と同じタトゥーポリーペクトミー部位
小さいポリープではスネアを最適に配置し、ポリープを静かに持ち上げることで粘膜下層の巻き込みを回避できるが、大きいポリープの切除では不可避となることがある。 上記の手技が適用されるが、ポリープを含む粘膜を剥がした後でも、巻き込まれた粘膜下層がスネアをポリペクトミー部位から切り離せないことがしばしばある。 このような場合、無理にスネアを引っ張る必要はありません。 スネアを少し開き、巻き込まれた粘膜下層の上を滑らせることで、スネアと剥がれたがまだ付着しているように見えるポリープを含む粘膜をポリペクトミー部位から離脱させることができます。 このような大きなポリープの巻き込まれた粘膜下層は、しばしば厚い偽茎を形成するが、粘膜下層の損傷は最小限にとどまる。
一度に切除できないさらに大きなポリープに対しては、EMSによる断片的ポリペクトミーが行われることがある。 EMSは粘膜下層の損傷がないため、従来のコールドスネアポリペクトミーやホットスネアポリペクトミーと比較して、ポリペクトミー部位の出血や変形が少なく、残存ポリープ組織がよく見えるため、ポリープの完全除去が容易になります(図2)<4853><8038>成果評価<178><2801>1. EMS採用前と後の全結腸ポリプと非節状結腸ポリプにおける入院必要な後出血率<4853><3027>2. 国内学会のガイドラインで推奨される間隔で、ポリペクトミー部位の生検とフォローアップ大腸内視鏡検査時の検査によって決定されるEMSポリープ除去の完全性(13、14)。
大腸内視鏡検査
大腸内視鏡検査は、ほとんどの症例で硬度可変式大腸内視鏡(PCF160、CF160、PCF180、CF180;オリンパス株式会社、東京、日本)を、数例でFUSEフルスペクトル大腸内視鏡(EndoChoice、Alpharetta、Georgia)を試験の一環として使用した。 ポリペクトミーは主にオーバルスネア(100600から100602、ConMed、Utica、NY)、少数例でスパイラルスネア(SD-230U-20、Olympus Corp、Tokyo、日本)、Exactoスネア(BX00711115、US Endoscopy、Mentor、OH)で施行された。
MNGI品質測定の一環として、2014年と2016年のZJCの年間大腸内視鏡検査統計は、盲腸到達率99.5-100%、スクリーニング大腸検査腺腫性ポリープ検出率男性50.3-60.1%、42.と報告された。女性1-54.0%
統計解析
統計解析はフィッシャーの正確検定を用いて行った。
結果
EMS Prevented Hospitalization-Requiring Postpolypectomy Bleeding
12年間にMNGI外来内視鏡センターでZJCが行ったスネアポリペクトミー付きの大腸内視鏡5142件をEMS時代以前(2005-2012、n=2973)とEMS時代(2013-2016、n=2169)に分類した(表1)。 最後の入院を必要とするポリープ切除後の出血は2012年9月に発生した。 EMS時代には1件もなかった(率0%)のに対し、EMS以前の時代には10件(ペダンセルポリープ2件を含む)見つかった(率0.336%)。 入院は大腸内視鏡検査後 1~16 日後に発生した。 この差は統計学的に有意であり(P = 0.0055)、pedunculated polypの2例を除いても(P = 0.012)有意差が保たれていた。 12年間のポリペクトミー後の出血例と全スネアポリペクトミー(CPTコード#45385)例
出血例12件のうち、合計18件のポリープが切除された。 2-3mmの管状腺腫(TA)をコールドスネアで切除した以外は、すべてホットスネアで切除した。 その内訳は、8~40mmのTA10個(11~15mmと36~40mmのペダンセル型ポリープ2個を含む)、25mmのtubulovillous adenoma(TVA)1個、6~10mmの無柄鋸歯状腺腫(SSA)4個、5mmのlipoma1個である。 切除したポリープの一部しか回収できず、粘膜下層を顕微鏡で確認できなかった1例を除き、残りの9例では図3Cに示すように、粘膜下層の焼灼を認め、焼灼端付近に血管が確認できることが多い。 これらの所見から,ホットスネアポリペクトミー時の粘膜下層の損傷がポリペクトミー後の出血に関与していることが示唆された。 EMSとホットスネアポリペクトミーで切除した進行性ポリープの病理組織学的比較。 (A,B)EMSで切除したポリープは一般的に粘膜下層が少なく、血管がないため粘膜の深い部分を示している。 (C)ホットスネアで切除したポリープの低倍率写真では、焼灼による組織損傷で典型的な粘膜下層が認められる
比較として、EMSで切除した進行大腸ポリープ20例の連続した顕微鏡観察も行っている。 これらのポリープには、さまざまな量の粘膜筋と、あったとしてもわずかな粘膜下層しかなく、血管はなかった(表2、図3A,B)。 これらの所見から,EMSは粘膜下層の損傷を回避することでポリープ切除後の出血を予防できることが示された(表2)。 EMSを用いて切除した進行性大腸ポリープ連続20例の特徴
EMS Facilitated Complete Polypectomy
EMSによる内視鏡的完全切除後に無作為に選んだ進行ポリープ10部位の縁(x4)と偽茎(x1)に広範囲生検が実施された。 どのサンプルにもポリープの残渣は認められなかった。 進行したポリープを除去した23人の患者の38のポリープ切除部位を含む、97の腫瘍性EMSポリペクトミー部位を6カ月から4年間追跡調査した。 59箇所の非進行性腫瘍性ポリープ(< 10mmで進行性の特徴がない)部位には、フォローアップの大腸内視鏡検査で残存または再発したポリープはなかった。 進行したポリープの大部分(38箇所中33箇所、87%)には、追跡調査の大腸内視鏡検査でポリープが認められなかった(表3)。 1年後、12番のポリープの近くに2個の小さなポリープが見つかったが、元のポリープとは異なるタイプであった(SSA vs. TA)。 ポリープ#13, #22, #25 については、1-3.5 年後のフォローアップ大腸内視鏡検査で、元のポリープ切除部位の近傍にそれぞれ 1 個の小さな (2-5 mm) 同種のポリープ (TA) が認められたが、これらはすべて、初回とフォローアップ大腸内視鏡を合わせて、24、10、14個の腺腫性ポリープが切除されたポリープ症例の発生で、新たにできたものか残留のものか判断は困難であった。 また、フォローアップ大腸内視鏡検査において、13番と25番のポリープの切除部位の近くに、TAとは異なるタイプの小さなポリープが発見されたことから、ポリープ切除が不完全だったのではなく、新たにポリープが成長したことが示唆された。 14ヶ月後、50mmの平坦なSSA(#26)の刺青のあるポリペクトミー部位に近い折り目の後ろに、10mmのSSAが発見された。 これは、元のポリープが非常に大きかったため、不完全なポリペクトミーである可能性もあるが、後屈で最もよく見える襞の裏側にあるため、最初の大腸内視鏡検査で見逃された拡大した別のポリープである可能性もある(図4)。 このように、EMSで切除された腫瘍性ポリープのうち97分の4(4.1%)、進行したポリープのうち38分の4(10.5%)が不完全なポリペクトミーであり、納得できる症例は1つもない。 これらの割合は、従来のスネアポリペクトミー技術で報告されたもの(18)と比べて非常に良好であった
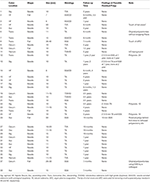
Table 3. EMSを用いて切除された進行性大腸ポリープ38例(23例)の追跡調査
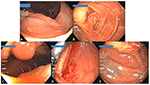
Figure 4. (A)上行結腸近位部の50mm大の無柄な鋸歯状腺腫(表3のPolyp#26)、背景にはICVが見える(矢印)。 (B)14ヶ月後のポリペクトミー部位の概要で、右側にタトゥーの1つが見える(矢印)。 (C)ポリペクトミー部付近の襞(矢印)に隠れた10mmのSSA。 (D) (C)のポリープのポリペクトミー部位を後方視したもの。 (E)タトゥーの1つ(左下)と(C)のポリープが隠れていた折り目(矢印)の相対的なスペース
考察
我々のデータ解析は、EMSが従来のスネアポリペクトミー技術に比べポリペクトミー後の出血を防ぎ完全なポリープ除去を容易にしたことを確認した。 したがって、EMSは大腸内視鏡検査をより安全で効果的な大腸がん予防ツールとすることができる。
ポリペクトミー後の出血や穿孔などの大腸内視鏡合併症は、粘膜下層や深部組織の損傷により発生する。 粘膜下層は結合組織や血管が豊富であるため,前癌の大腸ポリープを切除する際には,このような損傷は必要なく,避けるべきであろう。 スネアポリープ切除時に粘膜下層が巻き込まれることが多く、ギロチンや熱凝固を行わないとスネアを完全に閉鎖することができない。 TCSP法では、巻き込まれた組織全体をギロチンするため、ホットスネア法に比べて巻き込まれた粘膜下層へのダメージは少ないが(39)、巻き込まれた粘膜下層を損傷する。 TCSPではクリップなどの止血処置が必要なため、出血率が高くなり、ポリープ残渣の検出が困難になるだけでなく、大きなポリープへの適用が制限される(39-42)。 EMSは粘膜下層の完全切断を避けることで、即時および遅延出血を防ぎ、抗凝固療法や抗血小板療法を停止しなくても、大きなポリープに対して安全と思われる(図5)

Figure 5.粘膜下層の完全切断を避けた場合のEMSの効果 (A)細胞学的異形成を伴う15mm径の横行結腸無節性鋸歯状腺腫(表3のPolyp#7)。 (B)(A)のポリープ摘出直後のポリペクトミー部位。 (C)6ヶ月後の(B)と同じポリープ切除部位。 この患者はポリープ切除時にClopidogrelを中止していない。 EMSの安全性を考慮し、高齢(80歳まであと4ヶ月)であること、曲がりくねった長い大腸で便秘があることから、再度の大腸内視鏡検査が困難である可能性を考慮し、ポリープ切除を進めることにした。
潜在的な懸念は、EMSポリペクトリーの完全性、特に仮性包茎である。 私たちのポリペクトミー部位の生検データや、コールドスネアポリペクトミー後の偽茎の他の人の分析(43)では、ポリープが完全に除去されていることが示された。 このことは、追跡調査の大腸内視鏡検査でEMSポリペクトミー部位に残存ポリープの可能性が検出された頻度(おそらく0%、多くても4.1%の全腫瘍性ポリープまたは10.5%の進行ポリープ)が、以前の報告(18)よりはるかに低いことからもさらに支持されている。 Pohlらは、内視鏡的に「完全な」ポリペクトミーの端のサンプリングに基づき、全ポリペクトミーの10.1%に予想外の新生物が残存し、10-20mmの新生物ポリープの17.3%、TAよりもSSAの率が高く(31対7.2%)、大型(10-20mm)SSA全摘出が不完全だった47.6%と報告している(18)。 Zhangらは同様にポリープ(6-9mm)の不完全なTCSP(平均8.5%、断片的切除では13%)を報告し、クリッピングを要する即時出血がポリープごと、患者ごとにそれぞれ1.8%と2.7%で発生した(40)。 この差は、EMSポリペクトミーが従来のコールドスネアポリペクトミーやホットスネアポリペクトミーと比較して、出血や変形が少なく、外傷が少なかったためであると思われます。 これにより、ポリープ残渣の発見と除去が容易になっただけでなく、出血やその他の合併症を心配することなく、より寛大な粘膜切除が可能になった。 完全なポリペクトミーは、全大腸がんの2.6~9.0%を占めるインターバル型大腸がんの予防に重要である(19)。
切除されたポリープは粘膜下層の損傷が不可避なため、ポリペクトミー後の出血リスクが高いと思われる。 ZJCでは、切除位置を大腸壁から離し、茎部のポリープに近づけるようにしたため、経験の蓄積により、これらの稀なポリープからの出血が減少した可能性がある。 しかし、EMSの前後でペダンセルポリープからのポリペクトミー後の出血の減少は、統計的に有意ではなかった。
このように、EMSを行うことにより、非結節性ポリープからのポリペクトミー後の出血をなくすことができたと考えられる。 しかし、無傷の粘膜下層があるため、血腫が拡大したり失血したりすることはない。
EMRに比べEMSははるかに容易であり,側方に広がった大きな病変(表3)であっても,追加設備なしで同じポリペクトミー結果が得られ,出血リスクもはるかに軽減される. EMSは粘膜のみを切除するため、粘膜下層への浸潤を伴う早期がんは対象外であり、EMRと比較するためにはさらなる研究が必要である。 注目すべきは、研究期間中に10mmの未発癌大腸無柄ポリープに遭遇した1例である。 興味深いことに、ポリープ切除部位は滲出し続け、ヘモクリッピングを必要とした。 診断がついたのはポリープを切除した後であり、その後、患者は発症することなく外科に紹介された。 この症例では、拡大ピットパターン診断が事前診断に有用であった可能性があり、癌性ポリープを切らないよう、EMSの前に必ずポリープの慎重な検査を行うことが奨励される。 しかし、本症例では有害事象は発生しなかった。
EMSはスパイラルスネアやエキゾクトスネアを用い、粘膜下注入による粘膜挙上、アルゴンプラズマ凝固、ホットスネアチップ切除を併用して施行することがある。
EMSはかなりの数のMNGIの仲間に採用されましたが(表3、#37-38)、その利点の一般化にはさらなる確認研究が必要です。 それにもかかわらず、この比較的単純でありながら効果的なポリープ切除技術の革新は、大腸内視鏡によるより安全で効果的な大腸がん予防の新しいフロンティアを示す可能性がある。
Ethics Statement
この後ろ向き研究は、Sterling IRB (www.) によって2016年5月12日にIRB審査判定からの免除(IRB ID:5502)が承認された。sterlingirb.com)により承認されたプロトコル「Clinical and Histopathological Review of Mucosal Stripping as a Colonoscopy Polypectomy Technical Innovation」とMinnesota Gastroenterology Quality Committeeの勧告に従って実施されたものである。 また、ヘルシンキ宣言に基づき、全ての被験者が大腸内視鏡検査と治療に対してインフォームドコンセントを行った。
利益相反声明
著者は、本研究が潜在的な利益相反と解釈される商業的または金銭的関係がない状態で行われたことを宣言している。
謝辞
Douglas Nelson MD, Robert Ganz MD, John Allen MD, David Lieberman MD, Douglas Rex MD, Linda Rabeneck MD, Aasma Shaukat MD, Zong-ming Eric Chen MD PhD, Jeffrey Rank MD, Joshua Colton MD, Cecil Chally MDより批判的レビューと有益な示唆をいただいたことに感謝の意を表します。 Zengri WangとYongquan Xue PhDは統計解析に協力、Brian Hardwigはビデオ録画の設定に協力、Carlie Leyde, Amy Lounsbury, Martha Carland, JaNelle Gorg, Siri McCord, Karen Lang, Marit Brokは事務局として支援した。 また、Minnesota Gastroenterologyの内視鏡検査看護師のEMSポリペクトミーアシストに感謝する
本調査の予備的知見のポスターは、米国シカゴで開催された2017 DDWで発表された。 ポスターの要旨はGastrointestinal Endoscopy 2017; 85:AB520に掲載されました。
補足資料
本論文の補足資料は、以下のオンラインサイトに掲載されています。 https://www.frontiersin.org/articles/10.3389/fmed.2018.00312/full#supplementary-material
略語
EMS、内視鏡的粘膜剥離術、EMR、内視鏡的粘膜切除術、ESD、内視鏡的粘膜下層剥離術、TCSP、従来のコールドスネアポリス切除術。 TA, 管状腺腫; TVA(HD), 管状腺腫(高悪性度異形成あり); SSA(CD), 無柄鋸歯状腺腫(細胞学的異形成あり); UC, 潰瘍性大腸炎.
1. Winawer SJ, Zauber AG, Ho MN, O’Brien MJ, Gottlieb LS, Sternberg SS, et al. 大腸内視鏡的ポリープ切除による大腸癌予防。 全米ポリープ研究ワークグループ。 N Engl J Med. (1993) 329:1977-81. doi: 10.1056/NEJM199312303292701
PubMed Abstract | CrossRef Full Text | Google Scholar
2.大腸切除術による大腸癌の予防。 Zauber AG, Winawer SJ, O’Brien MJ, Lansdorp-Vogelaar I, van Ballegooijen M, Hankey BF, et al. 大腸切除術と大腸がん死亡の長期予防効果. N Engl J Med. (2012) 366:687-96. doi: 10.1056/NEJMoa1100370
PubMed Abstract | CrossRef Full Text | Google Scholar
3. Nishihara R, Wu K, Lochhead P, Morikawa T, Liao X, Qian ZR, et al. Lower endoscopy後の長期大腸癌発生と死亡率。 N Engl J Med. (2013) 369:1095-105. doi: 10.1056/NEJMoa1301969
PubMed Abstract | CrossRef Full Text | Google Scholar
4.大腸癌の長期的な発生率と死亡率。 Amri R, Bordeianou LG, Sylla P, Berger DL. 大腸がん手術におけるスクリーニング大腸内視鏡検査の成績に与える影響。 JAMA Surg. (2013) 148:747-54. doi: 10.1001/jamasurg.2013.8
PubMed Abstract | CrossRef Full Text | Google Scholar
5.大腸癌の手術におけるスクリーニング大腸内視鏡の影響。 Brenner H, Stock C, Hoffmeister M. Screening Sigmoidoscopy and Screening Colonoscopy on colorectal cancer incidence and mortality: systematic review and meta-analysis of randomised controlled trials and observational studies.スクリーニングS状結腸鏡検査とスクリーニング結腸鏡検査の大腸がん発症率と死亡率への影響:無作為化対照試験と観察研究の系統的レビューとメタ分析。 BMJ (2014) 348:g2467-78. doi: 10.1136/bmj.g2467
PubMed Abstract | CrossRef Full Text | Google Scholar
6.大腸癌の発生率と死亡率に対するスクリーニング大腸内視鏡検査の効果:無作為対照試験と観察研究のシステマティックレビューとメタアナリシス。 Sonnenberg A, Delcò F, Inadomi JM. 大腸癌のスクリーニングにおける大腸内視鏡検査の費用対効果。 Ann Intern Med. (2000) 133:573-84. doi: 10.7326/0003-4819-133-8-200010170-00007
PubMed Abstract | CrossRef Full Text | Google Scholar
7. Lansdorp-Vogelaar I, Knudsen AB, Brenner H. Colorectal cancer screening.Cost-effectiveness of Cost-Offectiveness. Epidemiol Rev. (2011) 33:88-100. doi: 10.1093/epirev/mxr004
PubMed Abstract | CrossRef Full Text | Google Scholar
8.大腸がん検診の費用対効果について。 Lieberman DA 平均的なリスクを持つ個人における大腸癌のスクリーニング:現在の方法と新たな問題点。 JAMA Intern Med. (2014) 174:10-11. doi: 10.1001/jamainternmed.2013.11499
PubMed Abstract | CrossRef Full Text | Google Scholar
9.大腸がんのスクリーニング:現在の方法と新たな問題。 Barclay RL, Vicari JJ, Doughty AS, Johanson JF, Greenlaw RL. スクリーニング大腸内視鏡検査における大腸内視鏡の抜去時間と腺腫の検出。 N Engl J Med. (2006) 355:2533-41. doi: 10.1056/NEJMoa055498
PubMed Abstract | CrossRef Full Text | Google Scholar
10.大腸内視鏡検査における大腸内視鏡の離脱時間と腺腫検出。 Kaminski MF, Regula J, Kraszewska E, Polkowski M, Wojciechowska U, Didkowska J, et al. 大腸内視鏡検査の品質指標とインターバル癌のリスク。 N Engl J Med. (2010) 362:1795-803. doi: 10.1056/NEJMoa0907667
PubMed Abstract | CrossRef Full Text | Google Scholar
11.大腸内視鏡検査の品質指標と間隔癌のリスク。 Corley DA, Jensen CD, Marks AR, Zhao WK, Lee JK, Doubeni CA, et al. アデノーマ検出率と大腸がんおよび死亡のリスク。 N Engl J Med. (2014) 370:1298-306. doi: 10.1056/NEJMoa1309086
CrossRef Full Text | Google Scholar
12. van Rijn JC, Reitsma JB, Stoker J, Bossuyt PM, van Deventer SJ, Dekker E. Polyp miss rate determined by Tandem colonoscopy: a systematic review. Am J Gastroenterol. (2006) 101:343-50. doi: 10.1111/j.1572-0241.2006.00390.x
CrossRef Full Text | Google Scholar
13.大腸内視鏡検査によるポリープの見逃し率:系統的レビュー。 Lieberman DA, Rex DK, Winawer SJ, Giardiello FM, Johnson DA, Levin TR. 大腸内視鏡によるスクリーニングとポリペクトミー後のサーベイランスのためのガイドライン:大腸癌に関する米国複数学会タスクフォースによるコンセンサスアップデート。 Gastroenterology (2012) 143:844-57. doi: 10.1053/j.gastro.2012.06.001
PubMed Abstract | CrossRef Full Text | Google Scholar
14.大腸内視鏡検査に関するガイドライン(Guidelines for Colonoscopy Surveillance after Screening and Polypectomy: US multi-society task force by the consensus update by colorective cancer. Rex DK, Schoenfeld PS, Cohen J, Pike IM, Adler DG, Fennerty MB, et al.(レックス・ディーケー、シェーンフェルド・ピーエス、コーヘン・ジェイ、パイクIM、アドラーDG、フェナティMB、他)。 大腸内視鏡検査の品質指標。 Gastrointest Endosc. (2015) 81:31-53. doi: 10.1016/j.gie.2014.07.058
PubMed Abstract | CrossRef Full Text | Google Scholar
15.大腸内視鏡検査の品質指標. 大腸内視鏡検査:合併症のプロスペクティブレポート。 J Clin Gastroenterol. (1992) 15:347-51. doi: 10.1097/00004836-199212000-00018
PubMed Abstract | CrossRef Full Text | Google Scholar
16.大腸内視鏡検査:合併症のプロスペクティブレポート。 Ko CW, Dominitz JA. 大腸内視鏡検査の合併症:その程度と管理。 Gastrointest Endosc Clin N Am. (2010) 20:659-71. doi: 10.1016/j.giec.2010.07.005
PubMed Abstract | CrossRef Full Text | Google Scholar
17.大腸内視鏡検査の合併症:その規模と管理。 ASGE Standards of Practice Committee, Fisher, DA, Maple, JT, Ben-Menachem, T, Cash, BD, Decker, GA, et al.大腸内視鏡検査の合併症. Gastrointest Endosc. (2011) 74:745-52. doi: 10.1016/j.gie.2011.07.025
CrossRef Full Text | Google Scholar
18. Pohl H, Srivastava A, Bensen SP, Anderson P, Rothstein RI, Gordon SR, et al. 大腸内視鏡検査時の不完全なポリープ切除-完全腺腫切除(CARE)試験の結果。 Gastroenterology (2013) 144:74-80. doi: 10.1053/j.gastro.2012.09.043
PubMed Abstract | CrossRef Full Text | Google Scholar
19.消化器病学(Gastroenterology)(2013)144:74-80. アドラーJ、ロバートソンDJ。 大腸内視鏡検査後のインターバル大腸がん:説明と解決策を探る。 Am J Gastroenterol. (2015) 110:1657-64. doi: 10.1038/ajg.2015.365
PubMed Abstract | CrossRef Full Text | Google Scholar
20.大腸内視鏡検査後の大腸がんのインターバル:説明と解決策を探る。 Ranasinghe I, Parzynski CS, Searfoss R, Montague J, Lin Z, Allen J, et al. 施設間の結腸鏡検査の質の違い:結腸鏡検査後の予定外の病院訪問のリスク標準化率の作成。 Gastroenterology (2016) 150:103-13. doi: 10.1053/j.gastro.2015.09.009
PubMed Abstract | CrossRef Full Text | Google Scholar
21.大腸内視鏡検査の施設間格差:大腸内視鏡検査後のリスク標準化率の開発. Rosen L, Bub DS, Reed JF, Nastasee SA. 大腸内視鏡下ポリープ切除術後の出血。 Dis Colon Rectum. (1993) 36:1126-31. doi: 10.1007/BF02052261
PubMed Abstract | CrossRef Full Text | Google Scholar
22.大腸切除術に伴う出血。 Gibbs DH, Opelka FG, Beck DE, Hicks TC, Timmcke AE, Gathright JB. ポリペクトミー後の大腸出血。 Dis Colon Rectum. (1996) 39:806-10. doi: 10.1007/BF02054448
PubMed Abstract | CrossRef Full Text | Google Scholar
23.大腸切除後の大腸出血。 Sorbi D, Norton I, Conio M, Balm R, Zinsmeister A, Gostout CJ. ポリペクトミー後の下部消化管出血:記述的分析。 Gastrointest Endosc. (2000) 51:690-6.105773
PubMed Abstract | CrossRef Full Text | Google Scholar
24. このような場合、医療従事者であれば、医療費負担を軽減するために、医療費負担の軽減を図ることができる。 Ann Intern Med. (2006) 145:880-6. doi: 10.7326/0003-4819-145-12-200612190-00004
PubMed Abstract | CrossRef Full Text | Google Scholar
25. Tolliver KA, Rex DK. 大腸内視鏡的ポリープ切除術。 胃腸薬クリノースアム。 (2008) 37:229-51, ix. doi: 10.1016/j.gtc.2007.12.009
PubMed Abstract | CrossRef Full Text | Google Scholar
26.大腸切除術(Polypectomy)。 Rabeneck L, Paszat LF, Hilsden RJ, Saskin R, Leddin D, Grunfeld E, et al. 外来結腸鏡検査後の出血と穿孔およびその危険因子の通常臨床での検討。 Gastroenterology (2008) 135:1899-906. doi: 10.1053/j.gastro.2008.08.058
PubMed Abstract | CrossRef Full Text | Google Scholar
27.大腸内視鏡検査後の出血と穿孔のリスク要因。 このような場合、医療従事者であることを証明する必要がある。 Ann Intern Med. (2009) 150:849-57. doi: 10.7326/0003-4819-150-12-200906160-00008
PubMed Abstract | CrossRef Full Text | Google Scholar
28.大腸内視鏡検査後の有害事象。 Sawhney MS, Salfiti N, Nelson DB, Lederle FA, Bond JH. 重篤なポリープ切除後遅発性出血のリスクファクター。 Endoscopy (2008) 40:115-9. doi: 10.1055/s-2007-966959
PubMed Abstract | CrossRef Full Text | Google Scholar
29.ポリープ切除後出血のリスクファクター(Endoscopy). 大腸病変の内視鏡的粘膜切除術後の出血を予測する因子。 Endoscopy (2011) 43:506-11. doi: 10.1055/s-0030-1256346
PubMed Abstract | CrossRef Full Text | Google Scholar
30.内視鏡的粘膜切除術後の出血を予測する因子。 大腸病変の広視野内視鏡切除術後の臨床的重大出血の予測:臨床的リスクスコア。 Am J Gastroenterol. (2016) 111:1115-22. doi: 10.1038/ajg.2016.235
PubMed Abstract | CrossRef Full Text | Google Scholar
31.大腸切除後の臨床的重大出血の予測:臨床的リスク・スコア. Albéniz E, Fraile M, Ibáñez B, Alonso-Aguirre P, Martínez-Ares D, Soto S, et al. 大腸病変の内視鏡的粘膜切除後の遅延出血のリスクを判断するスコアリングシステム. Clin Gastroenterol Hepatol. (2016) 14:1140-7. doi: 10.1016/j.cgh.2016.03.021
PubMed Abstract | CrossRef Full Text | Google Scholar
32.内視鏡的粘膜切除術後の出血遅延リスクを判定するスコアリングシステム(Scoring System)。 Wolff WI, Shinya H. 大腸内視鏡検査(colonoscopy)による大腸癌の早期診断. Cancer (1974) 34:912-34.
Google Scholar
33.大腸内視鏡検査による大腸癌の早期診断。 Tedesco FJ. 大腸内視鏡的ポリープ切除術。 で。 Silvia SE, editor. このような場合、「臓器移植」と呼ばれる。 Waye JD. ポリペクトミー-基本原則。 で。 において:において,Waye JD, Rex DK, Williams CB, editors. 大腸内視鏡検査の原理と実際. において,Waye JD, Rex DK, Williams CB, editors: doi: 10.1002/9780470986943.ch35
CrossRef Full Text | Google Scholar
35.大腸内視鏡検査-基本原則. Waye JD. ポリペクトミー:基本原則。 で。 Waye JD, Rex DK, Williams CB, editors. 大腸内視鏡検査の原理と実際. このような場合、「痒いところに手が届く」「痒いところに手が届く」「痒いところに手が届く」「痒いところに手が届く」「痒いところに手が届く」「痒いところに手が届く」「痒いところに手が届く」「痒いところに手が届く」「痒いところに手が届く」「痒いところに手が届く」「痒いところに手が届く」。 Meeroff JC. 大腸中皮ポリープをジアテルミーなしで除去する。 Gastrointest Endosc。 (1989) 35:136. doi: 10.1016/S0016-5107(89)72740-1
PubMed Abstract | CrossRef Full Text | Google Scholar
37.大腸中膜ポリープの除去。 大腸ポリープのコールドスネア切除術。 Gastrointest Endosc. (1992) 38:310-3. doi: 10.1016/S0016-5107(92)70422-2
PubMed Abstract | CrossRef Full Text | Google Scholar
38.コールドスネア切除術は、大腸ポリープを切除する。 チェンZJ.・バッツK.P. (2017). Mo2011 内視鏡的粘膜剥離術(EMS)によるポリープ切除後の出血の排除とより完全なポリープ切除の実現。 Gastroenterol. Endos. 85(Suppl.5):AB520に掲載されました。 Abstract Mo2011. doi: 10.1016/j.gie.2017.03.1198
CrossRef Full Text | Google Scholar
39.齋藤 孝(日本消化器内視鏡学会). 堀内明彦、中山雄一、梶山正樹、田中直樹、佐野恭子、グラハムDY. 抗凝固療法患者における小腸ポリープの切除:コールドスネア法と従来のポリープ切除法のプロスペクティブ・ランダマイズ比較. Gastrointest Endosc. (2014) 79:417-23. doi: 10.1016/j.gie.2013.08.040
PubMed Abstract | CrossRef Full Text | Google Scholar
40.をご参照ください。 大腸ポリープの内視鏡的完全切除のためのポリペクトミー。 Gastrointest Endosc. (2017). 87(3):733-740. doi: 10.1016/j.gie.2017.06.010
PubMed Abstract | CrossRef Full Text | Google Scholar
41. Paspatis GA, Tribonias G, Konstantinidis K, Theodoropoulou A, Vardas E, Voudoukis E, et al. 小型大腸ポリープにおけるポリペクトミー後の出血の発生におけるコールドスネアポリペクトミーとホットスネアポリペクトミーの前向き無作為比較。 Colorectal Dis. (2011) 13:e345-8. doi: 10.1111/j.1463-1318.2011.02696.x
PubMed Abstract | CrossRef Full Text | Google Scholar
42.大腸ポリープのポリープ切除後の出血の発生に関する前向き無作為化比較。 この論文では、大腸内視鏡検査における<10mmポリープに対するコールドポリペクトミーの安全性:前向き多施設研究。 内視鏡検査。 (2012) 44:27-31. doi: 10.1055/s-0031-1291387
PubMed Abstract | CrossRef Full Text | Google Scholar
43. Tutticci N, Burgess NG, Pellise M, Mcleod D, Bourke MJ. コールドスネアポリペクトミー後の粘膜欠損部における突起の特徴と意義。 Gastrointest Endosc. (2015) 82:523-8. doi: 10.1016/j.gie.2015.01.051
PubMed Abstract | CrossRef Full Text | Google Scholar