Tapwater bevat atmosferische gassen, zoals stikstof en zuurstof, die erin zijn opgelost. Als een glas gevuld met water een paar uur buiten staat, stijgt de temperatuur ervan enigszins (het water wordt warmer), waardoor de opgeloste gassen uit het water komen en bellen vormen aan de binnenkant van het glas.
Vul een glas met water (op of onder kamertemperatuur) en laat het een paar uur ongestoord staan (u kunt dit doen met kraanwater). Uiteindelijk zult u merken dat er heel kleine belletjes beginnen te ontstaan langs de zijkant van het glas (aan de binnenkant). Waarom gebeurt dit?

Oplosbaarheid van gassen in water
Het water dat uit kranen komt, gaat door leidingen voordat het in grote opslagtanks terechtkomt. Daarom staat het water onder een hogere druk dan normaal (terwijl het in de leidingen zit), en is het ook koeler. Deze twee omstandigheden zijn ideaal voor het oplossen van bepaalde gassen die veel voorkomen in onze atmosfeer, waaronder stikstof en zuurstof.
Gassen zijn beter oplosbaar in water bij koudere temperaturen
Gassen, in het algemeen, zijn beter oplosbaar in water wanneer het een lagere temperatuur heeft. Met andere woorden, je kunt zeggen dat de oplosbaarheid van gassen in water afneemt als de temperatuur van het water stijgt. De onderstaande grafiek kan helpen om te visualiseren hoe de oplosbaarheid van gassen varieert met veranderende temperatuur.
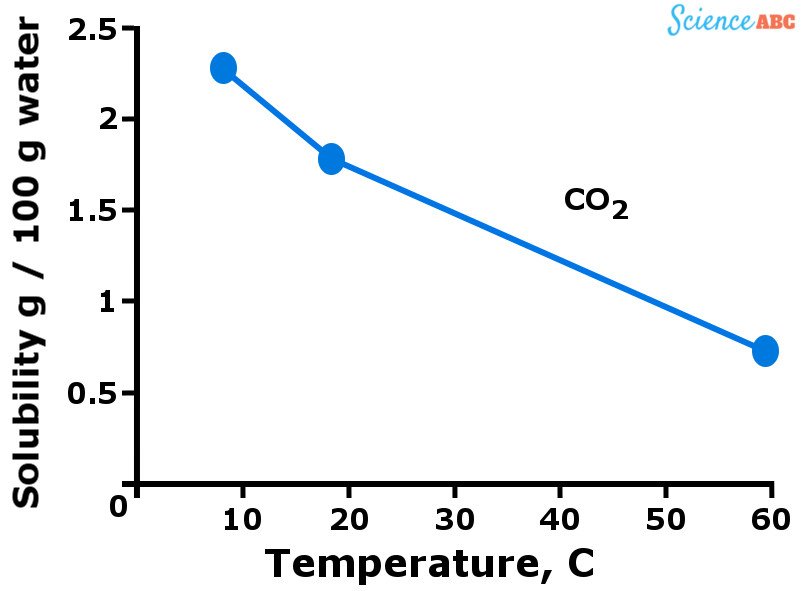
The variation of the solubility of carbon dioxide in water with increasing temperature
De neerwaartse trend van de oplosbaarheid van gassen met toenemende temperatuur is vrij vergelijkbaar met hoe de dampspanning toeneemt met de temperatuur. Er worden meer gasmoleculen opgelost in water als het koud is. Maar als water warmer wordt (d.w.z. als de temperatuur stijgt), neemt ook de kinetische energie van gasmoleculen toe.
Daardoor kunnen die moleculen vrijer bewegen en de intermoleculaire bindingen verbreken die hen bijeenhouden, zodat ze uit de oplossing ontsnappen. Daarom neemt de oplosbaarheid van gassen af als de temperatuur stijgt.
Gevaar voor waterleven door veranderende watertemperaturen
De temperatuurafhankelijkheid van de oplosbaarheid van gassen in water heeft een directe implicatie op het leven van waterdieren. Waterdieren zoals vissen hebben namelijk zuurstof nodig om te overleven, en die halen zij uit het water waarin zij leven door de opgeloste zuurstof (in het water) via hun kieuwen op te nemen. Aangezien zuurstof beter oplosbaar is in kouder water, is het van cruciaal belang dat de temperatuur niet boven een bepaalde grens stijgt.

Afvalproducten die vrijkomen bij energiecentrales doen de temperatuur van het water stijgen, waardoor het leven in zee gevaar loopt (Photo Credit : Flickr)
Dat is echter precies wat er tegenwoordig gebeurt, grotendeels als gevolg van menselijke activiteiten. Elektriciteitscentrales lozen bijvoorbeeld enorme hoeveelheden heet water in grote watermassa’s, waardoor de temperatuur van het water stijgt en het waterleven drastisch wordt beïnvloed. Dat is een zeer ongewenst gevolg van een dergelijke temperatuurafhankelijkheid van de oplosbaarheid van gassen.
De oplosbaarheid van gassen in water neemt toe met toenemende druk
Hoewel vloeistoffen en vaste stoffen vrijwel geen verandering van oplosbaarheid vertonen bij een veranderende druk van water, doen gassen dat wel. Er is waargenomen dat gassen bij hogere druk beter oplosbaar zijn in water. Koolzuurhoudende dranken zijn uitstekende voorbeelden van dit verschijnsel.
De wet van Henry
Het effect van een verandering in de druk van water op de oplosbaarheid van gassen kan worden verklaard door een van de gaswetten die bekend staat als de wet van Henry. Deze stelt dat “de hoeveelheid opgelost gas evenredig is met de partiële druk ervan in de gasfase”
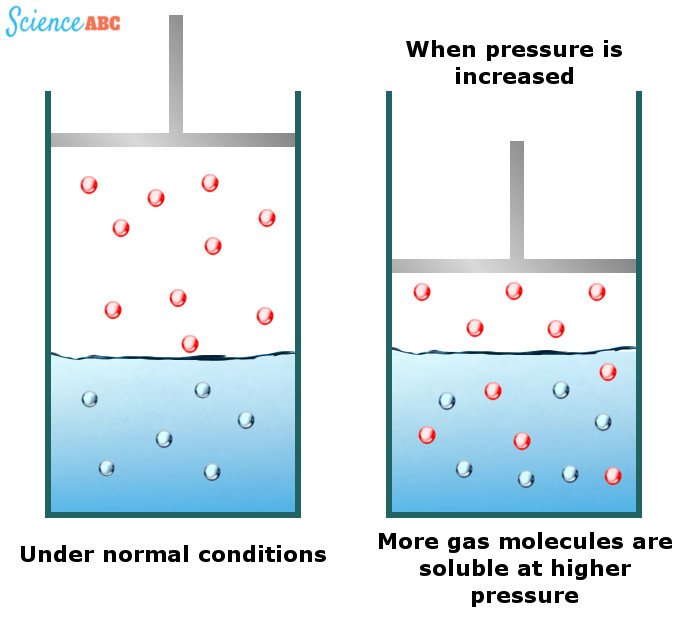
De eenvoudigste manier om deze afhankelijkheid te verklaren is dat wanneer de druk toeneemt, gasmoleculen in de oplossing worden geforceerd zodat de toegepaste druk kan worden verlicht. De volgende afbeelding moet helpen om dit beter te visualiseren:
Waarom er ’s nachts bellen ontstaan in een glas vol water
Door de twee fysische fenomenen die we hierboven hebben besproken, wordt leidingwater een goede kandidaat (zo niet ideaal) om opgeloste atmosferische gassen in vast te houden. Wanneer dat water echter in een glas wordt gegoten en een paar uur bij kamertemperatuur wordt gelaten, begint de druk af te nemen, terwijl de temperatuur begint te stijgen.

Een nacht lang vormen zich kleine belletjes in een glas water (Photo Credit : )
Daardoor komen de opgeloste gassen in het water uit de oplossing en vormen belletjes op de ruwe plekken aan de binnenkant van het glas. Aangezien het temperatuurverschil niet zo snel gaat (d.w.z. dat het water niet in een paar minuten van koud naar gloeiend heet gaat), duurt het een paar uur voordat de belletjes op het glas verschijnen.