Większość chemików potrafi wymienić artykuły, które ukształtowały ich życie. Dla wielu z nas jednym z najistotniejszych są zasady pierwszeństwa Cahn-Ingold-Prelog (CIP) z 1966 roku. Artykuł ten ma imponującą liczbę cytowań, ale równie ważna jest stabilność jego popularności: jego praktyczna użyteczność zapewniła, że jest on nadal używany przez pokolenia chemików na całym świecie.
Reguły CIP dają nam proste narzędzie do jednoznacznego opisu stereocentrów, i jako takie są istotną częścią naszej rygorystycznej nomenklatury cząsteczek. Jednak reguły te pozostają w tyle za niektórymi osiągnięciami w chemii, a w szczególności, gdy chodzi o gatunki supramolekularne.
Kowalencyjne wiązanie chemiczne jest często uważane za podstawę reguł CIP, ale niekowalencyjne oddziaływania, które są tak istotne dla chemii supramolekularnej, również powodują powstawanie centrów stereogenicznych. Oczywiście zasady można poprawić, ale powinniśmy również uważać, aby niepotrzebnie nie komplikować czegoś, co działa nadzwyczaj dobrze.
Istniejące zasady uwzględniają samotne pary – w 2004 roku Międzynarodowa Unia Chemii Czystej i Stosowanej (Iupac) zintegrowała je w odniesieniu do traktowania układów tetraedrycznych posiadających parę elektronów: „samotna para elektronów na atomie takim jak azot lub siarka ma fikcyjną liczbę atomową zero. Jest więc niżej notowana niż atom wodoru”. Proponujemy zatem dalsze, proste rozszerzenie reguł pierwszeństwa, aby rozwiązać problem oddziaływań niekowalencyjnych.
Nasz proponowany system
Dla oddziaływań z udziałem samotnych par proponujemy, aby skoordynowana samotna para miała przypisaną fikcyjną liczbę atomową pomiędzy 0 a 1 (innymi słowy większą niż nieskoordynowana samotna para, ale mniejszą niż atom wodoru). Jeśli jest więcej niż jedna skoordynowana samotna para, są one uporządkowane przez ligand zgodnie z klasycznymi regułami CIP.
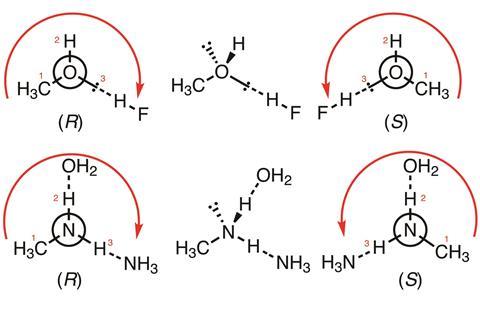
Powyższe przykłady pokazują, w jaki sposób byłoby przyznawane pierwszeństwo (zgodnie z czerwonymi liniami i liczbami) przy zastosowaniu proponowanych modyfikacji reguł CIP
W przypadku oddziaływań z udziałem atomów (na przykład atomy H jako część wiązań wodorowych), przyporządkowanie odbywa się według tych samych reguł, które stosuje się do centrów stereogenicznych; zatem, wiązanie wodorowe lub inne niekowalencyjne oddziaływanie ma wyższy priorytet niż wodór, a wiązania niekowalencyjne są uszeregowane według liczby atomowej liganda (od najwyższej do najniższej).
Powyżej są dwa proste przykłady, ze strzałkami i liczbami, aby wskazać kolejność pierwszeństwa. W pierwszym (kompleksy CH3OH:HF), koordynująca para samotna na metanolu ma pośredni priorytet pomiędzy niekoordynującą parą samotną (skierowaną do tyłu) a atomem wodoru; w drugim (kompleksy CH3NH2:NH3:OH2) wodór skoordynowany z tlenem ma wyższy priorytet niż skoordynowany z azotem. Oba mają wyższy priorytet niż para samotna (skierowana do tyłu), ale niższy niż grupa metylowa.
Poprawne nazwanie związku to uświadomienie sobie, że powstało centrum stereogeniczne i zadanie sobie pytania o pochodzenie chiralności; co więcej, obecność drugiego, supramolekularnego centrum stereogenicznego, powoduje ukryty diastereomeryzm. Ten prosty system pozwala nam na przejrzysty opis struktur supramolekularnych i dalsze ulepszanie języka chemii.