>
INTRODUÇÃO
>
De acordo com Torrent-Guasp e outros autores,1-6 o miocárdio ventricular consiste em uma banda contínua de músculo que se estende da raiz da artéria pulmonar até a raiz da aorta, formando uma estrutura helicoidal com 2 espirais e delimitando as 2 cavidades ventriculares. Esta banda miocárdica seria composta do “laço basal” e do “laço apical”. A alça basal é predominantemente horizontal e se divide em segmentos esquerdo e direito; a alça apical é predominantemente vertical e consiste do segmento descendente e do segmento ascendente (Figura 1). A ejeção seria produzida pela contração sucessiva dos segmentos basal direito e basal esquerdo, o que leva a um estreitamento da base do coração, seguido pela contração do segmento apical descendente. Isto, por sua vez, produz o encurtamento das dimensões longitudinais do coração, aproximando a base do ápice. O enchimento ventricular começaria com a contração do segmento apical ascendente, acompanhado do alongamento longitudinal e seguido do relaxamento das paredes ventriculares. Durante o ciclo cardíaco, o ápice permanece estacionário, enquanto a base se move para baixo, principal causa do encurtamento longitudinal e da ejeção do sangue, seguido de outro movimento ascendente ao qual é atribuída a aspiração do sangue do átrio esquerdo.7-9
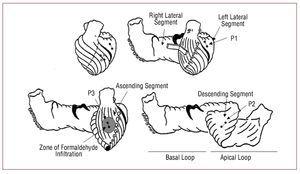
Figura 1. Diagramas mostrando os segmentos da banda miocárdica (Torrent-Guasp) e a posição dos pares de cristais implantados no miocárdio, representados como pequenos círculos conectados por uma linha. No diagrama superior esquerdo, os cristais correspondentes ao subendocárdio P2 (no segmento descendente do laço apical) são representados por círculos abertos.
Na doutrina clássica, o enchimento ventricular esquerdo começa com o relaxamento ventricular, um processo ativo de consumo de energia que reduz a pressão intraventricular a menos do que a correspondente ao átrio esquerdo. O cruzamento entre as pressões provoca a abertura da válvula mitral e o início do enchimento rápido precoce. Os fatores que determinam este mecanismo são considerados recuperação elástica, que envolve diferentes componentes como o conteúdo de elastina no colágeno da matriz extracelular,10 ou a titina proteica, que restaura a força ao sarcômero para sua recuperação após a deformação produzida durante a sístole,11 e o relaxamento da parede miocárdica. Hemodinamicamente, isto envolve 80% do volume de enchimento e é produzido com quase nenhuma contribuição de fatores atriais.10
O que é difícil de imaginar e demonstrar é o fato de que a fase de relaxamento isovoluminal e o subsequente enchimento rápido são conseqüência da contração da porção final da banda miocárdica. Entretanto, isto explicaria porque sempre que a disfunção sistólica se desenvolve, ela é acompanhada de disfunção diastólica, porque o índice T (a constante de tempo da queda de pressão durante a fase de contração isovolumiana) depende da contratilidade, e é melhorada pelo isoproterenol,12 e até porque a disfunção diastólica com função sistólica normal ou “preservada” é uma entidade para a qual o significado, a identificação e o tratamento permanecem pouco claros.13-17
Os estudos experimentais que aqui apresentamos foram realizados com o propósito de determinar os mecanismos miocárdicos envolvidos no fluxo transmissível diastólico precoce. Especificamente, desejamos saber se a fase de enchimento rápido ventricular é um processo de relaxamento ou contração.18 Para abordar esta questão, vamos examinar se a contração do segmento ascendente da alça apical coincide temporalmente com a chamada fase de relaxamento isovolumico ventricular esquerdo e se a indução de hipocinesia ou acinesia limitada a esse segmento tem um efeito negativo no fluxo transmitral precoce, a taxa de queda da pressão intraventricular durante a fase isovolumica e a pressão mínima alcançada no ventrículo esquerdo.
MÉTODOS
Estudamos 12 suínos de ambos os sexos com peso médio de 28,2 (5,1) kg. Eles haviam sido criados na Unidade Veterinária do Centro de Pesquisa do nosso hospital. As experiências foram realizadas de acordo com as directrizes espanholas e europeias para a “Protecção de animais utilizados para fins experimentais e outros fins científicos” (Real Decreto 223/1988 e Real Decreto 1201/2005). Os procedimentos cirúrgicos foram realizados por investigadores que possuíam o certificado europeu de formação em experimentação animal (Real Decreto 1201/2005).
Preparação das Experiências
No dia da experiência, os animais são pré-anestesiados e sedados nas suas baias por injecção intramuscular de midazolam (0,5 mg/kg de peso corporal) e ketamina (10 mg/kg de peso corporal). A anestesia é induzida na sala de operação experimental pela via intravenosa (tiopental, 10 mg/kg de peso corporal), e a intubação endotraqueal e cateterização da veia jugular externa são realizadas. A anestesia é mantida com sevoflurano (2,5%) em uma mistura de 40% de oxigênio e 60% de óxido nitroso, administrado por meio de um ventilador (Temel VT3, Espanha). A analgesia e relaxamento são iniciados com brometo de vecurônio (0,08 mg/kg de peso corporal) e cloridrato de morfina (0,7 mg/kg de peso corporal) e são mantidos com brometo de vecurônio (0,08 mg/kg de peso corporal) e 20 mg de cloridrato de morfina em 50 mL de soro em uma bomba de infusão a uma taxa de 12 mL/h. É realizada esternotomia mediana, seguida de pericardiectomia. A ventilação mecânica é ajustada a uma taxa entre 16 e 20 respirações por minuto e a um fluxo de gás de aproximadamente 5 L/min, dependendo das oximetrias no sangue. O eletrocardiograma periférico, pH do sangue, gases do sangue, hematócrito e temperatura retal são monitorados durante todo o experimento. A temperatura é mantida com uma manta elétrica.
Função Segmental
Três pares de microcristais ultra-sônicos (Biopac Systems, Santa Barbara, California, EUA) são implantados no miocárdio: um par no mesocárdio (a uma profundidade de aproximadamente 4 a 5 mm) do aspecto lateral do ventrículo esquerdo correspondente à alça basal, segmento lateral esquerdo (P1), seguindo a direção do eixo longitudinal do coração; outro par no subendocárdio do aspecto anterior do terço médio do ventrículo esquerdo, entre o primeiro e segundo ramos diagonais da artéria descendente anterior e tangencial a ela, zona correspondente ao segmento descendente da alça apical (P2); e, finalmente, outro par no subepicárdio (a uma profundidade de 1 a 2 mm) do aspecto anterior do ventrículo esquerdo, entre o primeiro e segundo ramos diagonais da artéria descendente anterior e paralelo à artéria descendente anterior em direção à raiz da aorta, numa zona correspondente ao segmento ascendente da alça apical (P3) (Figura 1). Os pares de microcristais são alinhados seguindo a direção das fibras musculares da zona em que são colocados. Eles são separados por aproximadamente 2 cm. Os pares P2 são ancorados no subendocárdio por meio de punção transseptal, alcançando a cavidade ventricular e voltando para trás a fim de depositá-los no subendocárdio, formando uma cruz com os pares P3 no subepicárdio. Os pares de cristais nos permitem conhecer o deslocamento relativo dos 2 pontos do miocárdio sobre os quais estão fixados e, portanto, as propriedades dinâmicas do segmento contido entre eles. A aquisição das curvas regionais de contratilidade miocárdica é realizada com o Sistema Digital de Medição Ultrassônica da Sonometrics Corporation (Londres, Ontário, Canadá).
Pressão intracavitária
Um cateter é inserido através da parede livre do ventrículo esquerdo para monitorização da pressão ventricular esquerda e outro é inserido através da aurícula para medir a pressão atrial esquerda; ambos os cateteres são conectados a transdutores de pressão (Transpac IV, EUA).
Fluxo aórtico
A raiz aórtica é dissecada e um medidor de fluxo eletromagnético é colocado (Transonic Systems, New York, Estados Unidos).
Fluxo Transmitral
Foi realizado um ecocardiograma Doppler (Interspec XL Doppler, EUA) com uma sonda de 5-MHz, diretamente sobre o epicárdio, para registrar o fluxo transmitral a partir de uma visão apical de quatro câmaras, primeiro em condições basais e, em seguida, após a injeção de formaldeído diluído na parede miocárdica.
Indução de Akinesia Segmental
O que envolve injeções de formaldeído19 diluído a 2,5%, usando uma agulha atraumática, no subepicárdio (a uma profundidade de 1 a 2 mm) do segmento ascendente da alça apical, onde se encontram os pares de cristais P2. Injecta-se um máximo de 0,8 mL da diluição indicada, distribuídos entre 3 e 4 injecções. Após cada injeção, o efeito produzido na fração de encurtamento do segmento é monitorado até que a akinesia ou discinesia seja alcançada no segmento em questão.
Recolha de dados
Os registros correspondentes: ECG (I, II, ou III), pressão ventricular esquerda em mm Hg, pressão atrial esquerda em mm Hg, fluxo aórtico (mL/min) e dados sonométricos dos 3 segmentos de banda miocárdica indicados são digitalizados e armazenados em memória eletrônica (BIOPAC Systems Inc, Santa Bárbara, Califórnia, Estados Unidos). As curvas de velocidade de fluxo de transmissão e os valores obtidos através do ecodopplercardiograma (m/s) são armazenados separadamente.
Após a conclusão dos experimentos, os animais são sacrificados sob anestesia por meio de injeção intravenosa de cloreto de potássio. Após a remoção da estrutura anatômica (o coração), verifica-se o sítio anatômico dos 3 pares de cristais, disseca-se a parede anterior do ventrículo esquerdo, seguindo a via da artéria interventricular, e verifica-se a profundidade em que cada cristal é implantado, assim como a região do músculo infiltrado com formaldeído.
Parâmetros Analisados
No ecodopplercardiograma com Doppler, estudamos as velocidades máximas de fluxo transmissível no início (E) e final (A) da diástole e a relação E/A. As curvas de pressão intracavitária fornecem a pressão sistólica ventricular esquerda máxima, a pressão ventricular esquerda mínima, a pressão diastólica final do ventrículo esquerdo (PEDVE), o tempo decorrido desde o fechamento da valva aórtica até que a pressão intraventricular supere em 10 mm Hg a pressão diastólica final, o que corresponde ao tempo de relaxamento isovolumico12; neste ponto, podemos ter certeza de que esta é a fase isovolumica com a valva mitral ainda fechada. As curvas de função segmentar revelam a fração de encurtamento, e as curvas de fluxo aórtico mostram o fluxo aórtico médio e a relação temporal entre o final da contração de cada um dos três segmentos (P1, P2 e P3) e a suspensão do fluxo aórtico (tempo de fechamento aórtico-contração P1, P2, P3). Todos estes parâmetros são analisados antes e depois da injeção de formaldeído no segmento ascendente. A fração de encurtamento é medida após cada injeção de formaldeído até que uma mudança adequada no segmento injetado seja verificada.
Análise dos Resultados
As variáveis estudadas são contínuas, e os resultados são expressos como a média mais ou menos o desvio padrão. As mudanças nas variáveis após o bloqueio com formaldeído em relação às condições de linha de base foram estudadas. A comparação das médias foi realizada pelo teste t de Student para amostras pareadas ou pelo teste não paramétrico de Mann-Whitney para dados que não apresentaram uma distribuição normal. Um valor de P inferior a 0,05 foi considerado significativo. Foi utilizado o pacote estatístico SPSS (versão 9.0).
RESULTADOS
Mudanças hemodinâmicas (Tabela 1)
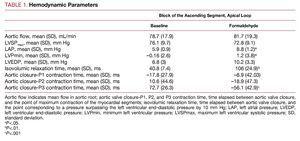
A injeção de formaldeído prolonga significativamente o tempo necessário para superar a pressão diastólica final do ventrículo esquerdo em 10 mm Hg após o fechamento da valva aórtica, aumenta a pressão ventricular esquerda mínima que é alcançada na diástole precoce, passando de pressões negativas para positivas, aumenta – embora não de forma muito significativa – o PEDVE e incrementa significativamente a pressão atrial média. Não há alterações significativas imediatas no fluxo aórtico ou na pressão ventricular esquerda durante a sístole (Figura 2).
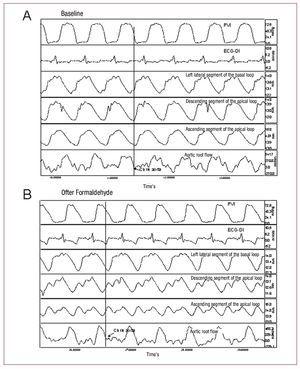
Figura 2. Registro da pressão ventricular esquerda (IVP); eletrocardiograma (ECG-DI); contratilidade segmentar no segmento lateral esquerdo da alça basal, segmento descendente da alça apical e segmento ascendente da alça apical; e fluxo radicular aórtico em condições basais (A) e após injeção de formaldeído (B). As setas indicam os pontos correspondentes ao fechamento da válvula aórtica. As alterações induzidas pela injeção de formaldeído estão descritas no texto.
Fim da Contração Miocárdica e Iniciação da Diástase
Para determinar o início da fase de relaxamento isovoluminal, identificamos o momento em que a ejeção do sangue cessa na curva de fluxo aórtico e a fase de contração segmentar nas curvas sonométricas correspondentes (Figura 2).
Em todos os experimentos, o segmento ascendente (P3) estava em contração após a interrupção do fluxo aórtico e o fechamento da válvula aórtica. A contração do último segmento miocárdico terminou em um tempo médio de 72,7 (26,3) ms após o fechamento da válvula aórtica, coincidindo com a chamada fase de relaxamento isovolumico no início da diástole (Figura 2), enquanto que o segmento descendente (P2) atingiu contração máxima de 10,6 (44,6) ms após o fechamento da válvula aórtica, e o final da contração do segmento P1 (alça basal) precedeu o fechamento da válvula aórtica (Tabela 1).
Fluxo Transmitral
Tabela 2 mostra o efeito produzido na fração de encurtamento do segmento monitorado pela injeção de formaldeído no segmento ascendente da alça apical. Há uma diminuição dos níveis de discinesia (segundo protocolo) no segmento injetado (P3, segmento ascendente) e hipocinesia no segmento vizinho, o segmento descendente (P2) da alça apical. As zonas correspondentes ao segmento lateral esquerdo do laço basal (P1) não são alteradas. Em paralelo, o fluxo transmitral é afetado, com alterações nas taxas de enchimento ventricular na diástole precoce e na relação E/A; a onda E diminuiu à medida que a onda A aumentou, sendo a relação E/A significativamente reduzida (P
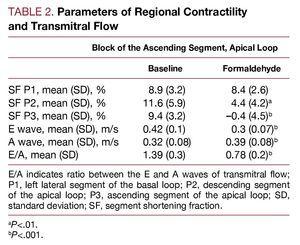
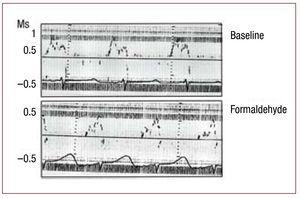
Figura 3. Alterações imediatas na taxa de fluxo transmitral, medida pelo ecodopplercardiograma, secundária à infiltração com formaldeído a 2,5% no segmento ascendente da alça apical. Figura corrigida para reprodução.
DISCUSSÃO
Quando o ventrículo deixa de ejetar o sangue, a sístole termina e inicia-se a diástole. A partir deste momento, e até a abertura da válvula mitral, há um período de tempo durante o qual ambas as válvulas são fechadas, o que é conhecido como fase de relaxamento isovoluminal. Durante esta fase, a pressão intraventricular cai a um ritmo constante12 e leva a gradientes de pressão transmural e transvalvar em direção ao interior da câmara. É produzido um efeito de sucção, ao qual é imediatamente atribuída a rapidez do enchimento ventricular precoce e cuja perda total ou parcial é causa de disfunção diastólica do ventrículo esquerdo, o substrato fisiopatológico da insuficiência cardíaca com função sistólica preservada.
Na prática clínica,16,20,21 o diagnóstico de insuficiência cardíaca por disfunção diastólica depende de 3 condições: presença de sinais ou sintomas de insuficiência cardíaca, fração de ejeção ventricular esquerda normal ou levemente diminuída e aumento da pressão de enchimento ventricular esquerdo. Este último fator tem impacto e pode ser medido na curva de enchimento ventricular esquerdo do ecodopplercardiograma, no prolongamento do período de relaxamento isovolumérico, na diminuição da velocidade diastólica precoce (E), no prolongamento do tempo de desaceleração, no aumento da velocidade diastólica final (A) e na redução da relação E/A.
O preenchimento ventricular, que identifica o tempo diastólico, foi atribuído à contração atrial até 1954.3,4 Aceita-se agora que o ventrículo esquerdo participe ativamente com a força de sucção a que nos referimos acima. Trata-se de um processo ativo22,23 que consome energia e envolve a troca de Ca2+. Vários autores consideram a diástole uma conseqüência do alongamento das fibras miocárdicas das paredes de uma câmara fechada. Seria um fenômeno ligado ao relaxamento muscular (separação dos filamentos de miosina) e à recuperação elástica das fibras, em que intervém a elastina contida em uma rede de colágeno que compõe o tecido conjuntivo extrafibrilar, bem como a titina protéica como elemento de recuperação do sarcômero deformado durante a sístole.10,11 A ativação mecânica ventricular durante a diástole é heterogênea, com gradientes de relaxamento subendocárdico-subepicárdico no início da diástole.22,24,25
Na teoria de Torrent-Guasp, é um fenômeno sistólico ligado à contração muscular.23,26 A ejeção do sangue é conseqüência da contração do segmento descendente da alça apical; sua contração “parafusa” a base sobre o ápice, aproximando as 2 partes. O segmento seguinte e final da banda muscular é o segmento ascendente da alça apical, que cobre o segmento descendente, formando o epicárdio do aspecto anterior até a raiz da aorta, e que foi “esticado e enroscado” pela contração do segmento anterior. Quando se contrai, o segmento ascendente faz um movimento que “desatarraxa” a base, afastando-a do ápice, aumentando o eixo longitudinal do coração e produzindo sucção como a que ocorreria no interior de um cilindro que se afasta de seu pistão, dinâmica que tem sido observada em humanos em imagens de ressonância magnética.27
Neste estudo, contribuímos com dados que demonstram que a força de sucção produzida durante a fase de relaxamento isovolumérico depende da contração porque é produzida durante a fase de contração segmentar e, além disso, que sua funcionalidade está fortemente ligada à contração do segmento ascendente do laço apical, especificamente:
1. Mostramos que, no início e durante a fase de relaxamento isovolumico do ventrículo esquerdo, o segmento ascendente da alça apical está se contraindo.
2. A infiltração do segmento ascendente da alça apical com formaldeído diluído afeta diretamente a capacidade de reduzir a pressão intraventricular ou, em outras palavras, a força de sucção. Este aspecto tem sido demonstrado pelo prolongamento do tempo necessário para que a pressão intraventricular caia para 10 mm Hg sobre a pressão diastólica final, um nível que nos permite assegurar que a válvula mitral ainda esteja fechada e que a menor velocidade (ou seja, mais tempo decorrido) na queda de pressão esteja em uma câmara fechada (isovolúmica). Também tem sido demonstrado pela menor pressão intraventricular mínima atingida na diástole precoce, que é significativamente afetada quando nos infiltramos no referido segmento ascendente.
Limitações do Estudo
O uso de cristais ultra-sônicos é apropriado se assumirmos que a estrutura do miocárdio está organizada parcial ou totalmente em uma banda e que implantamos os cristais ultra-sônicos na mesma linha que marca a direção do movimento das fibras. Este método é incapaz de isolar a função de um único segmento, pois faz parte do mesmo continuum que os outros. Assim, a alteração de qualquer segmento alteraria a contração em toda a faixa, como ocorre em nosso modelo, no qual a injeção no segmento ascendente também modifica significativamente a contração das fibras contidas no P2, identificado como pertencente ao segmento descendente, que é vizinho ao segmento injetado.
Para a identificação dos segmentos e a direção de suas fibras, bem como a confirmação post-mortem nos espécimes anatômicos, fomos aconselhados pelo Dr. Torrent-Guasp. As fibras subendocárdicas do segmento descendente na zona do aspecto anterior do ventrículo esquerdo passam pelo mesocárdio a uma certa profundidade, cruzando-se perpendicularmente com as do segmento ascendente28, circunstância que temos confirmado nas peças anatômicas. Por esta razão, os cristais ancorados no subendocárdio seguiram uma direção que o par implantado no epicárdio correspondente (segmento ascendente) cruzou perpendicularmente.
O envolvimento muscular secundário à injeção de formaldeído diluído é difícil de padronizar e, naturalmente, afeta todas as propriedades ativas e passivas da fibra, reduzindo a contração, relaxamento e elasticidade aos seus limites mais baixos. A tentativa tem sido feita para minimizar as alterações produzidas pelo formaldeído, limitando a quantidade e o número de injeções em todos os experimentos e monitorando o efeito dependendo da alteração da contratilidade do segmento injetado e verificando a alteração no fluxo transmitral. Para muitos pesquisadores, as teorias do Dr. Torrent-Guasp abriram caminhos que eles podem seguir para progredir na compreensão da fisiologia do músculo cardíaco. Outros pontos continuam sendo de difícil conciliação com dados anteriores.18
CONCLUSÕES
Nesta nova concepção da função diastólica, as 3 propriedades das fibras miocárdicas participariam, seguindo uma certa ordem e, ao mesmo tempo, sobrepondo-se. A aspiração inicial com a câmara fechada seria conseqüência da contração do último segmento da banda, como tentamos demonstrar com os experimentos aqui apresentados; o relaxamento das fibras dos segmentos sucessivos com a válvula mitral aberta permitiria o preenchimento rápido e, finalmente, a distensibilidade permitiria que a parede miocárdica cedesse em resposta ao aumento de pressão/volume produzido pela injeção no átrio.
ACKNOWLEDGMENTS
Este estudo foi realizado em memória do Dr. Francisco Torrent-Guasp.
Este estudo foi financiado pelo subsídio nº 99/1002 do Fondo de Investigaciones Sanitarias (FIS) espanhol.