INTRODUCERE
Potrivit lui Torrent-Guasp și altor autori,1-6 miocardul ventricular este format dintr-o bandă continuă de mușchi care se întinde de la rădăcina arterei pulmonare până la rădăcina aortică, formând o structură elicoidală cu 2 spirale și delimitând cele 2 cavități ventriculare. Această bandă miocardică ar fi compusă din „bucla bazală” și „bucla apicală”. Bucla bazală este predominant orizontală și se împarte în segmente stâng și drept; bucla apicală este predominant verticală și este formată din segmentul descendent și segmentul ascendent (figura 1). Ejecția ar fi produsă prin contracția succesivă a segmentelor bazal drept și bazal stâng, ceea ce duce la o îngustare a bazei inimii, urmată de contracția segmentului apical descendent. Aceasta, la rândul său, produce scurtarea dimensiunilor longitudinale ale inimii, aducând baza mai aproape de apex. Umplerea ventriculară ar începe cu contracția segmentului apical ascendent, însoțită de alungirea longitudinală și urmată de relaxarea pereților ventriculari. În timpul ciclului cardiac, apexul rămâne staționar, în timp ce baza se deplasează în jos, principala cauză a scurtării longitudinale și a ejecției sângelui, urmată de o altă mișcare ascendentă căreia i se atribuie aspirarea sângelui din atriul stâng. 7-9
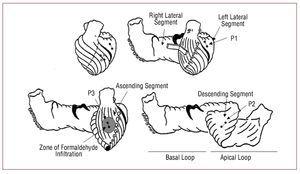
Figura 1. Diagrame care prezintă segmentele benzii miocardice (Torrent-Guasp) și poziția perechilor de cristale implantate în miocard, reprezentate sub forma unor mici cercuri conectate de o linie. În diagrama din stânga sus, cristalele corespunzătoare subendocardului P2 (în segmentul descendent al buclei apicale) sunt reprezentate prin cercuri deschise.
În doctrina clasică, umplerea ventriculului stâng începe cu relaxarea ventriculară, un proces activ consumator de energie care reduce presiunea intraventriculară la o valoare mai mică decât cea corespunzătoare atriului stâng. Trecerea dintre presiuni determină deschiderea valvei mitrale și inițierea umplerii rapide timpurii. Factorii care determină acest mecanism sunt considerați a fi recuperarea elastică, care implică diferite componente, cum ar fi conținutul de elastină din colagenul din matricea extracelulară,10 sau proteina titină, care redă forța sarcomerului pentru recuperarea acestuia după deformarea produsă în timpul sistolei,11 și relaxarea peretelui miocardic. Din punct de vedere hemodinamic, aceasta implică 80% din volumul de umplere și este produsă cu o contribuție aproape nulă din partea factorilor atriali.10
Ceea ce este greu de imaginat și de demonstrat este faptul că faza de relaxare izovolumică și umplerea rapidă ulterioară sunt o consecință a contracției porțiunii finale a benzii miocardice. Totuși, acest lucru ar explica de ce ori de câte ori apare o disfuncție sistolică, aceasta este însoțită de o disfuncție diastolică, de ce indicele T (constanta de timp a căderii presiunii în timpul fazei de contracție izovolumică) depinde de contractilitate și este îmbunătățită de izoproterenol12 și chiar de ce disfuncția diastolică cu funcție sistolică normală sau „conservată” este o entitate a cărei semnificație, identificare și tratament rămân neclare13-17.
Studiile experimentale pe care le prezentăm aici au fost efectuate cu scopul de a determina mecanismele miocardice implicate în fluxul transmisibil diastolic precoce. În mod specific, am dorit să știm dacă faza de umplere rapidă a ventriculului este un proces de relaxare sau de contracție.18 Pentru a răspunde la această întrebare, vom examina dacă contracția segmentului ascendent al ansei apicale coincide temporal cu așa-numita fază de relaxare izovolumică a ventriculului stâng și dacă inducerea hipochineziei sau achineziei limitate la acest segment are un efect negativ asupra fluxului transmitral precoce, a ratei de scădere a presiunii intraventriculare în timpul fazei izovolumice și a presiunii minime atinse în ventriculul stâng.
METODE
Am studiat 12 porci de ambele sexe cu o greutate medie de 28,2 (5,1) kg. Aceștia fuseseră crescuți în Unitatea Veterinară a Centrului de Cercetare al spitalului nostru. Experimentele au fost efectuate în conformitate cu orientările spaniole și europene pentru „Protecția animalelor utilizate în scopuri experimentale și în alte scopuri științifice” (Decretul regal 223/1988 și Decretul regal 1201/2005). Procedurile chirurgicale au fost efectuate de către investigatori care dețineau certificatul european de formare în domeniul experimentelor pe animale (Decretul regal 1201/2005).
Pregătirea experimentelor
În ziua experimentului, animalele sunt preanesteziate și sedate în grajdurile lor prin injectare intramusculară de midazolam (0,5 mg/kg de greutate corporală) și ketamină (10 mg/kg de greutate corporală). Anestezia este indusă în sala de operație experimentală pe cale intravenoasă (tiopental, 10 mg/kg greutate corporală) și se efectuează intubația endotraheală și cateterizarea venei jugulare externe. Anestezia este menținută cu sevofluran (2,5%) într-un amestec de 40% oxigen și 60% protoxid de azot, administrat cu ajutorul unui ventilator (Temel VT3, Spania). Analgezia și relaxarea sunt inițiate cu bromură de vecuroniu (0,08 mg / kg de greutate corporală) și clorhidrat de morfină (0,7 mg / kg de greutate corporală) și sunt menținute cu bromură de vecuroniu (0,08 mg / kg de greutate corporală) și 20 mg de clorhidrat de morfină în 50 ml de ser într-o pompă de perfuzie cu o viteză de 12 ml / h. Se efectuează sternotomia mediană, urmată de pericardiectomie. Ventilația mecanică este ajustată la o rată între 16 și 20 de respirații pe minut și la un debit de gaze de aproximativ 5 L/min, în funcție de oximetria din sânge. Electrocardiograma periferică, pH-ul sângelui, gazele din sânge, hematocritul și temperatura rectală sunt monitorizate pe toată durata experimentului. Temperatura este menținută cu ajutorul unei pături electrice.
Funcția segmentară
Trei perechi de microcristale ultrasonice (Biopac Systems, Santa Barbara, California, SUA) sunt implantate în miocard: o pereche în mezocardul (la o adâncime de aproximativ 4 până la 5 mm) al feței laterale a ventriculului stâng, corespunzător ansei bazale, segmentul lateral stâng (P1), urmând direcția axei longitudinale a inimii; o altă pereche în subendocardul feței anterioare a treimii medii a ventriculului stâng, între prima și a doua ramură diagonală a arterei descendente anterioare și tangențial la aceasta, o zonă corespunzătoare segmentului descendent al ansei apicale (P2); și, în sfârșit, o altă pereche în subepicardul (la o adâncime de 1 până la 2 mm) al feței anterioare a ventriculului stâng, între prima și a doua ramură diagonală a arterei descendente anterioare și paralel cu artera descendentă anterioară spre rădăcina aortică, într-o zonă care corespunde segmentului ascendent al ansei apicale (P3) (figura 1). Perechile de microcristale sunt aliniate urmând direcția fibrelor musculare din zona în care sunt plasate. Acestea sunt separate de aproximativ 2 cm. Perechile P2 sunt ancorate în subendocard prin puncție transseptală, ajungând în cavitatea ventriculară și retrăgându-se pentru a le depune în subendocard, formând o cruce cu perechile P3 în subepicard. Perechile de cristale ne permit să cunoaștem deplasarea relativă a celor 2 puncte din miocard peste care sunt fixate și, astfel, proprietățile dinamice ale segmentului conținut între ele. Achiziționarea curbelor regionale de contractilitate miocardică se realizează cu ajutorul sistemului digital de măsurare cu ultrasunete Sonometrics Corporation (London, Ontario, Canada).
Presiuni intracavitare
Un cateter este introdus prin peretele liber al ventriculului stâng pentru monitorizarea presiunii ventriculare stângi și un altul este introdus prin auriculă pentru a măsura presiunea atrială stângă; ambele catetere sunt conectate la transductoare de presiune (Transpac IV, SUA).
Fluxul aortic
Se disecă rădăcina aortică și se plasează un debitmetru electromagnetic (Transonic Systems, New York, Statele Unite).
Fluxul transmisral
Se efectuează o ecocardiogramă Doppler (Interspec XL Doppler, SUA) cu o sondă de 5 MHz, direct deasupra epicardului, pentru a înregistra fluxul transmisral dintr-o vedere apicală cu patru camere, mai întâi în condiții de bază și apoi după injectarea de formaldehidă diluată în peretele miocardic.
Inducerea acineziei segmentare
Aceasta implică injecții de formaldehidă19 diluată la 2,5%, folosind un ac atraumatic, în subepicard (la o adâncime de 1 până la 2 mm) a segmentului ascendent al buclei apicale, unde sunt situate perechile de cristale P2. Se injectează maximum 0,8 ml din diluția indicată, distribuite în 3 și 4 injecții. După fiecare injecție, se monitorizează efectul produs asupra fracțiunii de scurtare a segmentului până când se obține akinezia sau diskinezia în segmentul dat.
Colectarea datelor
Înregistrările corespunzătoare la: ECG (I, II sau III), presiunea ventriculară stângă în mm Hg, presiunea atrială stângă în mm Hg, fluxul aortic (ml/min) și datele sonometrice ale celor 3 segmente de bandă miocardică indicate sunt digitizate și stocate într-o memorie electronică (BIOPAC Systems Inc, Santa Barbara, California, Statele Unite). Curbele vitezei fluxului transmitral și valorile obținute cu ajutorul ecocardiografiei Doppler (m/s) sunt stocate separat.
După finalizarea experimentelor, animalele sunt sacrificate sub anestezie prin intermediul unei injecții intravenoase de clorură de potasiu. După îndepărtarea structurii anatomice (inima), se verifică locul anatomic al celor 3 perechi de cristale, se disecă peretele ventricular stâng anterior, urmărindu-se traseul arterei interventriculare, și se verifică adâncimea la care este implantat fiecare cristal, precum și regiunea mușchiului infiltrată cu formaldehidă.
Parametrii analizați
În ecocardiograma Doppler, se studiază vitezele maxime ale fluxului transmitral la începutul (E) și la sfârșitul (A) diastolei și raportul E/A. Curbele de presiune intracavitară furnizează presiunea sistolică ventriculară stângă maximă, presiunea ventriculară stângă minimă, presiunea ventriculară stângă end-diastolică (LVEDP), timpul scurs de la închiderea valvei aortice până când presiunea intraventriculară depășește presiunea end-diastolică cu 10 mm Hg, ceea ce corespunde timpului de relaxare izovolumică12; în acest moment, putem fi siguri că este vorba de faza izovolumică cu valva mitrală încă închisă. Curbele funcției segmentare relevă fracția de scurtare, iar curbele fluxului aortic arată fluxul aortic mediu și relația temporală dintre sfârșitul contracției fiecăruia dintre cele trei segmente (P1, P2 și P3) și suspendarea fluxului aortic (timp închidere aortică-contracție aortică P1, P2, P3). Toți acești parametri sunt analizați înainte și după injectarea de formaldehidă în segmentul ascendent. Fracția de scurtare este măsurată după fiecare injecție de formaldehidă până când se verifică o modificare adecvată în segmentul injectat.
Analiza rezultatelor
Variabilele studiate sunt continue, iar rezultatele sunt exprimate ca medie plus sau minus deviația standard. Au fost studiate modificările variabilelor în urma blocării cu formaldehidă în raport cu condițiile inițiale. Compararea mediilor s-a realizat cu ajutorul testului Student t pentru eșantioane perechi sau al testului neparametric Mann-Whitney pentru datele care nu prezentau o distribuție normală. O valoare P mai mică de 0,05 a fost considerată semnificativă. A fost utilizat pachetul statistic SPSS (versiunea 9.0).
REZULTATE
Schimbări hemodinamice (Tabelul 1)
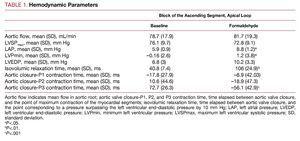
Injectarea de formaldehidă prelungește semnificativ timpul necesar pentru a depăși presiunea diastolică finală a ventriculului stâng cu 10 mm Hg după închiderea valvei aortice, mărește presiunea ventriculară stângă minimă care este atinsă în diastole timpurii, trecând de la presiuni negative la presiuni pozitive, crește – deși nu într-un mod foarte semnificativ – LVEDP și crește semnificativ presiunea atrială medie. Nu există modificări semnificative imediate ale fluxului aortic sau ale presiunii ventriculare stângi în timpul sistolei (figura 2).
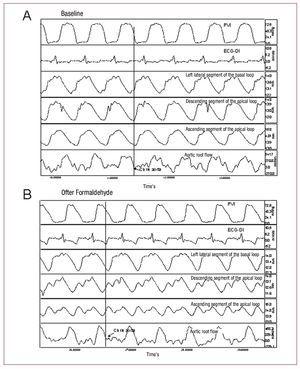
Figura 2. Înregistrarea presiunii ventriculare stângi (PVI); electrocardiograma (ECG-DI); contractilitatea segmentară în segmentul lateral stâng al ansei bazale, segmentul descendent al ansei apicale și segmentul ascendent al ansei apicale; și fluxul rădăcinii aortice în condiții de bază (A) și după injectarea de formaldehidă (B). Săgețile indică punctele care corespund închiderii valvei aortice. Modificările induse de injectarea formaldehidei sunt descrise în text.
Finalul contracției miocardice și inițierea diastolei
Pentru a determina inițierea fazei de relaxare izovolumică, am identificat momentul în care încetează ejecția de sânge în curba fluxului aortic și faza de contracție segmentară în curbele sonometrice corespunzătoare (figura 2).
În toate experimentele, segmentul ascendent (P3) a fost în contracție după ce fluxul aortic a încetat și valva aortică s-a închis. Contracția ultimului segment miocardic s-a încheiat într-un timp mediu de 72,7 (26,3) ms după închiderea valvei aortice, coincizând cu așa-numita fază de relaxare izovolumică în diastole timpurii (figura 2), în timp ce segmentul descendent (P2) a atins contracția maximă la 10,6 (44,6) ms după închiderea valvei aortice, iar sfârșitul contracției segmentului P1 (bucla bazală) a precedat închiderea valvei aortice (tabelul 1).
Fluxul transmisibil
Tabelul 2 arată efectul produs în fracția de scurtare a segmentului monitorizat prin injectarea de formaldehidă în segmentul ascendent al buclei apicale. Se observă o scădere până la niveluri de diskinezie (conform protocolului) în segmentul injectat (P3, segmentul ascendent) și hipocinezie în segmentul vecin, segmentul descendent (P2) al ansei apicale. Zonele corespunzătoare segmentului lateral stâng al buclei bazale (P1) nu sunt alterate. În paralel, fluxul transmitral este afectat, cu modificări ale ritmurilor de umplere ventriculară în diastole timpurii și ale raportului E/A; unda E a scăzut pe măsură ce unda A a crescut, raportul E/A fiind semnificativ redus (P
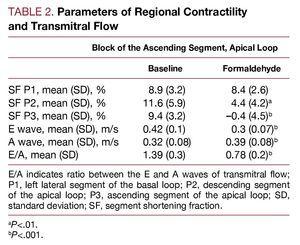
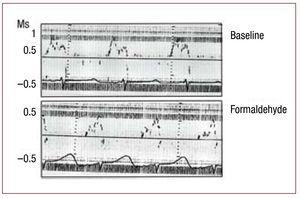
Figura 3. Modificări imediate ale debitului transmitral, măsurate prin ecocardiografie Doppler, secundare infiltrării cu formaldehidă 2,5% în segmentul ascendent al ansei apicale. Figura corectată pentru reproducere.
DISCUȚII
Când ventriculul încetează să mai evacueze sângele, se termină sistolele și începe diastolele. Din acest moment, și până la deschiderea valvei mitrale, există o perioadă de timp în care ambele valve sunt închise, care este cunoscută sub numele de faza de relaxare izovolumică. În timpul acestei faze, presiunea intraventriculară scade la o rată constantă12 și conduce la gradienți de presiune transmurală și transvalvulară spre interiorul camerei. Se produce un efect de aspirație, căruia i se atribuie imediat rapiditatea umplerii ventriculare precoce și a cărui pierdere totală sau parțială este o cauză a disfuncției diastolice ventriculare stângi, substratul fiziopatologic al insuficienței cardiace cu funcția sistolică păstrată.
În practica clinică,16,20,21 diagnosticul de insuficiență cardiacă datorată disfuncției diastolice depinde de 3 condiții: prezența semnelor sau simptomelor de insuficiență cardiacă, o fracție de ejecție ventriculară stângă normală sau ușor scăzută și o presiune de umplere ventriculară stângă crescută. Acest din urmă factor are un impact și poate fi măsurat în curba de umplere a ventriculului stâng din ecocardiograma Doppler, în prelungirea perioadei de relaxare izovolumică, în scăderea vitezei diastolice timpurii (E), în prelungirea timpului de decelerare, în creșterea vitezei diastolice finale (A) și în reducerea raportului E/A.
Luminația ventriculară, care identifică timpul diastolic, a fost atribuită contracției atriale până în 1954.3,4 Acum este acceptat faptul că ventriculul stâng participă activ cu forța de aspirație la care ne-am referit mai sus. Este un proces activ22,23 care consumă energie și implică schimbul de Ca2+. O serie de autori consideră că diastolele sunt o consecință a alungirea fibrelor miocardice ale pereților unei camere închise. Ar fi un fenomen legat de relaxarea musculară (separarea filamentelor de miozină) și de refacerea elastică a fibrelor, în care intervine elastina conținută într-o rețea de colagen care alcătuiește țesutul conjunctiv extrafibrilar, precum și proteina titină ca element de refacere a sarcomerului deformat în timpul sistolei10,11. Activarea mecanică ventriculară în timpul diastolei este eterogenă, cu gradienți de relaxare subendocardică-subepicardică la începutul diastolei.22,24,25
În teoria lui Torrent-Guasp, este un fenomen sistolic legat de contracția musculară.23,26 Ejecția sângelui este o consecință a contracției segmentului descendent al ansei apicale; contracția acestuia „înșurubează” baza peste apex, apropiind cele 2 părți. Următorul și ultimul segment al benzii musculare este segmentul ascendent al ansei apicale, care acoperă segmentul descendent, formând epicardul feței anterioare până la rădăcina aortică, și care a fost „întins și înfășurat” prin contracția segmentului precedent. Atunci când se contractă, segmentul ascendent face o mișcare care „deșurubează” baza, îndepărtând-o de apex, mărind axa longitudinală a inimii și producând o aspirație asemănătoare cu cea care ar avea loc în interiorul unui cilindru care se îndepărtează de pistonul său, dinamică care a fost observată la om în imaginile de rezonanță magnetică27.
În acest studiu, am contribuit cu date care demonstrează că forța de aspirație produsă în timpul fazei de relaxare izovolumică depinde de contracție, deoarece este produsă în timpul fazei de contracție segmentară și, mai mult, că funcționalitatea sa este puternic legată de contracția segmentului ascendent al ansei apicale, în mod specific:
1. Am demonstrat că, la începutul și în timpul fazei de relaxare izovolumică a ventriculului stâng, segmentul ascendent al buclei apicale se contractă.
2. Infiltrarea segmentului ascendent al buclei apicale cu formaldehidă diluată afectează în mod direct capacitatea de reducere a presiunii intraventriculare sau, cu alte cuvinte, forța de aspirație. Acest aspect a fost demonstrat prin prelungirea timpului necesar pentru ca presiunea intraventriculară să scadă până la 10 mm Hg peste presiunea diastolică finală, un nivel care ne permite să ne asigurăm că valva mitrală este încă închisă și că viteza mai mică (adică mai mult timp scurs) în căderea presiunii se află într-o cameră închisă (izovolumică). Aceasta a fost demonstrată și de presiunea intraventriculară minimă mai mică atinsă în diastole timpurii, care este semnificativ afectată atunci când infiltrăm respectivul segment ascendent.
3. Ca o consecință a unei viteze de cădere mai mici și a unei scăderi finale mai puțin accentuate a presiunii intraventriculare în timpul fazei izovolumice, efectul de aspirație este mai mic și rata de umplere ventriculară scade în timpul diastolei timpurii, crescând în compensație în timpul diastolei finale, ca o consecință a unei contracții a atriului stâng mai „plin”. Acest lucru a fost demonstrat de modificările valorilor lui E, A și ale raportului E/A, precum și de creșterea progresivă a presiunii atriale care începe în diastole timpurii.
Limitele studiului
Utilizarea cristalelor ultrasonice este adecvată dacă presupunem că structura miocardului este organizată parțial sau total în bandă și că am implantat cristalele ultrasonice în aceeași linie care marchează direcția de mișcare a fibrelor. Această metodă nu este în măsură să izoleze funcția unui singur segment, deoarece acesta face parte din același continuum ca și celelalte. Astfel, alterarea unui anumit segment ar modifica contracția în întreaga bandă, așa cum se întâmplă în modelul nostru, în care injectarea în segmentul ascendent modifică semnificativ și contracția fibrelor conținute în P2, identificate ca aparținând segmentului descendent, care se învecinează cu segmentul injectat.
Pentru identificarea segmentelor și a direcției fibrelor lor, precum și pentru confirmarea postmortem în specimenele anatomice, am fost consiliați de Dr. Torrent-Guasp. Fibrele subendocardice ale segmentului descendent din zona feței anterioare a ventriculului stâng trec prin mezocard la o anumită adâncime, încrucișându-se perpendicular cu cele ale segmentului ascendent28, împrejurare pe care am confirmat-o în probele anatomice. Din acest motiv, cristalele ancorate în subendocard, au urmat o direcție pe care perechea implantată în epicardul corespunzător (segmentul ascendent) o traversa perpendicular.
Aplicarea musculară secundară injecției de formaldehidă diluată este greu de standardizat și, bineînțeles, afectează toate proprietățile active și pasive ale fibrei, reducând contracția, relaxarea și elasticitatea la limitele lor cele mai joase. S-a încercat reducerea la minimum a modificărilor produse de formaldehidă, limitând cantitatea și numărul de injecții în toate experimentele și monitorizând efectul în funcție de alterarea contractilității segmentului injectat și verificarea modificării fluxului transmisibil. Pentru mulți cercetători, teoriile doctorului Torrent-Guasp au deschis căi pe care le pot urma pentru a progresa în înțelegerea fiziologiei mușchiului cardiac. Alte puncte continuă să fie greu de reconciliat cu datele anterioare.18
CONCLUZII
În această nouă concepție a funcției diastolice, cele 3 proprietăți ale fibrelor miocardice ar participa, urmând o anumită ordine și, în același timp, suprapunându-se. Aspirația inițială cu camera închisă ar fi o consecință a contracției ultimului segment al benzii, așa cum am încercat să demonstrăm prin experimentele prezentate aici; relaxarea fibrelor segmentelor succesive cu valva mitrală deschisă ar permite o umplere rapidă și, în sfârșit, distensibilitatea ar face posibilă cedarea peretelui miocardic ca răspuns la creșterea de presiune/volum produsă de injecția în atriu.
RECUNOȘTINȚE
Acest studiu a fost realizat în memoria Dr. Francisco Torrent-Guasp.
Acest studiu a fost finanțat prin grantul nr. 99/1002 de la Fondo de Investigaciones Sanitarias (FIS) din Spania.