L’uvea, una sezione altamente vascolarizzata dell’occhio situata sotto la sclera, fornisce alla maggior parte delle strutture oculari sostanze nutritive attraverso i rami anteriore e posteriore dell’arteria oftalmica.
L’uvea consiste di iride, corpo ciliare e coroide. L’iride controlla quanta luce entra nell’occhio, mentre il corpo ciliare produce l’umor acqueo e ne controlla il deflusso contraendo e allargando la rete trabecolare. Il corpo ciliare controlla anche l’accomodazione contraendosi e rilassandosi.
Il terzo elemento, la coroide, è un tessuto altamente vascolarizzato e pigmentato che fornisce nutrimento agli strati esterni della retina e assorbe la luce in eccesso. L’infiammazione di una qualsiasi di queste strutture è nota come uveite.
Un sinonimo di uveite è l’irite, e anche se l’irite è più specifica tecnicamente e anatomicamente, i medici spesso usano i termini in modo intercambiabile. La forma più comune di questa malattia è l’uveite anteriore non granulomatosa, che può presentarsi come unilaterale o bilaterale; cronica o acuta; e idiopatica, infettiva, immunologica o neoplastica.
I sintomi classici includono arrossamento, fotofobia e dolore spesso descritto come un dolore sordo; tuttavia, nelle forme croniche della malattia, questi sintomi possono essere completamente assenti. Spesso, un’anamnesi medica e oculare sufficiente può rivelare la causa precipitante, sebbene anche i test di laboratorio non possano scoprire l’eziologia sottostante in ogni caso.
In ogni caso, è importante classificare correttamente l’uveite per diagnosticare e trattare correttamente il paziente, eliminando così il potenziale di ulteriori complicazioni, compresa la cecità. Questo articolo esaminerà i segni e i sintomi tipici dell’uveite anteriore, oltre a discutere le considerazioni essenziali per il trattamento.
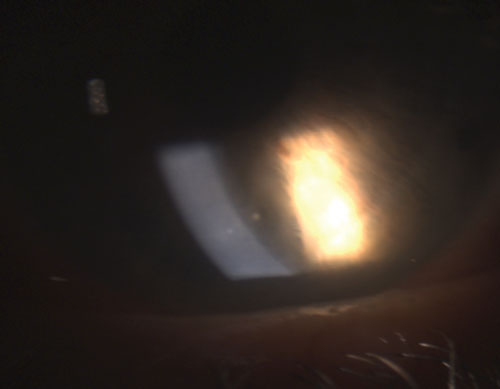
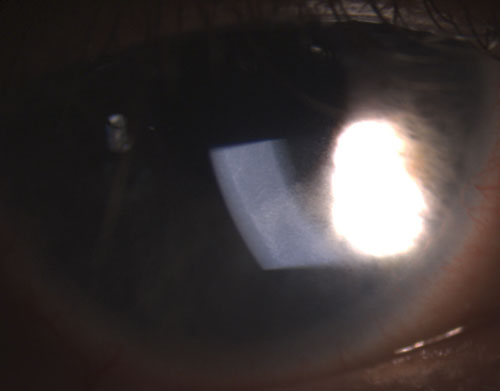
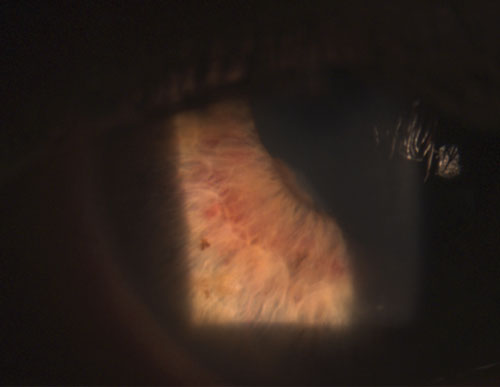
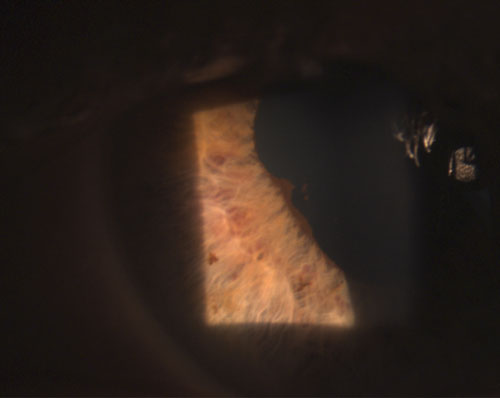
4. Sinechia posteriore parzialmente rotta dopo instillazione di fenilefrina 10% e atropina 1%.
Classificazione della malattia, workup e diagnosi
Quando si diagnostica l’uveite anteriore, è necessario considerare una varietà di segni e caratteristiche associate. Come precedentemente notato, i sintomi caratteristici includono dolore sotto forma di un dolore sordo, arrossamento e fotofobia. Visivamente, il consueto rossore ciliare (flush circumlimbale) è spesso visto e la pupilla può essere mediamente dilatata. Per una diagnosi ufficiale, tuttavia, le cellule devono essere viste nella camera anteriore e il flare può essere presente o meno. È importante notare che il flare a volte può essere visto nella camera anteriore quando non è presente un’infiammazione attiva, perché l’uveite cronica di lunga durata danneggia l’integrità della vascolarizzazione dell’iride e del corpo ciliare.1
Per diagnosticare e gestire correttamente l’uveite, è necessario prima classificarla. L’infiammazione anteriore limitata all’iride e alla camera anteriore è definita irite. Quando l’infiammazione coinvolge anche il corpo ciliare, come evidenziato dalla presenza di cellule vitree anteriori, si chiama iridociclite. Tuttavia, quando solo il corpo ciliare è infiammato, si chiama semplicemente ciclite (anche se questo di solito non è un termine clinicamente significativo). L’uveite intermedia, o pars planitis, comporta l’infiammazione della pars plana, la parte centrale del corpo ciliare. Aggregati di globuli bianchi, o opacità a palla di neve, accumulati vicino alla retina inferiore sono tipicamente visti nella pars planitis.1
L’uveite posteriore comporta l’infiammazione del segmento posteriore, compresa la retina, la coroide, il vitreo e talvolta la sclera, mentre la pan-uveite coinvolge tutte le strutture dell’uvea oltre ai tessuti adiacenti. Va notato che più l’uveite procede posteriormente nell’occhio, maggiore è il rischio di malattia sistemica associata, più sarà difficile da trattare e maggiore sarà il rischio di complicazioni. In ogni caso, la differenza tra la semantica specifica aiuta il medico con la diagnosi clinica e dirige l’attenzione alle aree appropriate di preoccupazione.
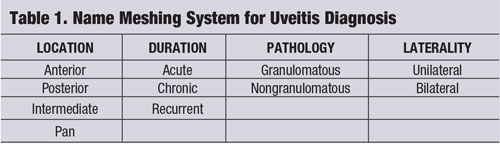
Una strategia di “name meshing” (vedi “Name Meshing System for Uveitis Diagnosis.”) è uno strumento che può essere utilizzato per focalizzare il pensiero clinico e fornire una valutazione e una gestione della malattia del paziente su misura e a costi contenuti.2-4 L’entità uveitica dovrebbe essere suddivisa in base alla sua localizzazione, durata, patologia e lateralità.1-4
In riferimento all’infiammazione oculare, “granulomatoso” si riferisce tipicamente a una forma più grave di uveite, con caratteristiche distintive come granulomi dell’iride, noduli di Koeppe sul margine pupillare, noduli di Busacca nello stroma dell’iride e precipitati cheratici (KP) sull’endotelio corneale che sono grandi, globulari e grassi, noti come KP di grasso di montone (figura 1).1-3,5 Un ipopion può formarsi nella camera anteriore se l’infiammazione rimane incontrollata.
Gli uveitidi granulomatosi più comuni includono tubercolosi, sarcoidosi e malattia di Lyme.2 L’infiammazione oculare non granulomatosa, d’altra parte, è meno grave ed è caratterizzata da KP più piccoli (figura 2), meno noduli (se presenti) e una minore probabilità di formazione di sinechie (figure 3 e 4).2,3 Nel complesso, l’uveite granulomatosa ha maggiori probabilità di essere associata a malattie sistemiche ed è più difficile da trattare con un rischio maggiore di complicazioni rispetto all’uveite non granulomatosa.
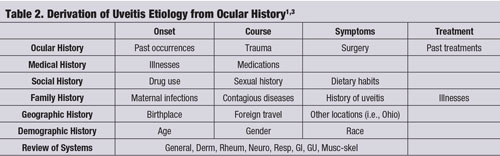
Frequentemente, un’anamnesi oculare specifica – insieme ad un attento esame con lampada a fessura – può portare all’eziologia corretta dell’uveite senza ulteriori test o studi di laboratorio. (Vedere “Derivazione dell’eziologia dell’uveite dall’anamnesi oculare”, pagina 60.)1
Il “sistema delle nove I”, che classifica l’infiammazione dei tessuti oculari in una voce specifica, è un altro utile strumento di classificazione (vedere “Il sistema delle nove “I”.”) Una qualsiasi delle nove “I” può essere la causa principale dell’uveite, e fino al 38% dei casi è idiopatico.6
Corde di sangue
L’uveite acuta non granulomatosa può essere associata all’antigene leucocitario umano B27 (HLA-B27). Altre entità che possono essere collegate all’HLA-B27 includono la sindrome di Reiter, la malattia infiammatoria della ciotola (cioè la colite ulcerosa o la malattia di Crohn), la spondilite anchilosante, la malattia di Behçet e l’artrite psoriasica.1,6,7 Queste entità sono solitamente anteriori e unilaterali. Altre uveitidi acute nongranulomatose includono la malattia di Lyme e i traumi. Le entità croniche nongranulomatose comuni includono l’artrite reumatoide giovanile e l’iridociclite eterocromica di Fuchs.3,4,6
L’uveite cronica è solitamente meno sintomatica delle presentazioni acute. Sebbene la sifilide sia tipicamente raggruppata nell’uveite granulomatosa cronica insieme alla sarcoidosi e alla tubercolosi, può presentarsi in una qualsiasi delle categorie come mascherata.4,6
Le uveiti posteriori includono la tubercolosi, la toxoplasmosi, l’istoplasmosi, la sarcoidosi e l’herpes – sebbene l’herpes sia spesso anche anteriore.3,6 Anche se di solito è posteriore, qualsiasi forma di uveite posteriore può raramente presentarsi anteriormente. Un’entità che può essere erroneamente classificata come uveite anteriore idiopatica è la crisi glaucomatocitica (cioè la sindrome di Posner-Schlossman).1 Si tratta classicamente di un occhio bianco con una lieve reazione della camera anteriore e una IOP molto elevata (da 30 mm Hg a 60 mm Hg). Tende ad essere unilaterale, ricorrente e relativamente asintomatica.1,5
Gli studi del sangue spesso devono essere ordinati nei casi in cui l’anamnesi e l’esame fisico non portano ad una diagnosi definitiva – specialmente in presenza di uveite bilaterale, granulomatosa o ricorrente.6 L’approccio “shotgun” è costoso, aspecifico e può essere facilmente evitato con abilità clinica astuta.

Ecco alcuni dei più comuni test di laboratorio utilizzati per aiutare a localizzare l’eziologia dell’uveite:6-8
– L’emocromo completo (CBC) con differenziale aiuta a determinare lo stato di salute generale del paziente e può aiutare a diagnosticare una varietà di disturbi, come anemia, infezioni e leucemia.
– La proteina C-reattiva (CRP) è un marcatore dell’infiammazione e serve a monitorare la risposta al trattamento.2,4 I test CRP non sono in grado di determinare la causa o la posizione dell’infiammazione all’interno del corpo, tuttavia.
– La velocità di eritrosedimentazione (VES) è tipicamente ordinata insieme a un test CRP. Una VES aiuta a rilevare l’infiammazione e serve a monitorare l’eziologia sottostante.
– Il test degli anticorpi antinucleari (ANA) serve a individuare alcuni disturbi autoimmuni come il lupus eritematoso sistemico, la sclerodermia, l’artrite giovanile, la polimiosite, le malattie infiammatorie intestinali e la psoriasi.
– Il test del fattore reumatoide (RF) può aiutare a diagnosticare l’artrite reumatoide e la sindrome di Sjögren, tra gli altri che a volte si sovrappongono al test ANA.
– Il Rapid plasma regain (RPR), il laboratorio di ricerca sulle malattie veneree (VDRL) e il test di assorbimento degli anticorpi treponemici fluorescenti (FTA-ABS) sono utilizzati per lo screening della sifilide. Il FTA-ABS è un test di 24 ore utilizzato per rilevare gli anticorpi al batterio Treponema pallidum e confermare la presenza di sifilide. L’FTA-ABS non indica se la malattia è attiva o inattiva, tuttavia, ed è tipicamente somministrato dopo un test di screening per la malattia attiva, RPR o VDRL. Sono disponibili altri test treponemici, come la microemoagglutinazione-Treponema pallidum (MHA-TP), il test di agglutinazione delle particelle di Treponema pallidum (TP-PA) e il test di emaglutinazione del Treponema pallidum (TPHA), ma non sono così comunemente noti nelle comunità di cura degli occhi come FTA-ABS.
|
Sia la RPR che la VDRL sono tipicamente positive nella sifilide primaria e secondaria e negative nella sifilide terziaria (latente) e dopo un trattamento efficace della malattia.4 La RPR è comunemente scelta rispetto alla VDRL perché è più facile da somministrare e meno costosa. Falsi positivi possono verificarsi, tuttavia, con entrambi i test. Le entità che possono disturbare l’accuratezza dei risultati includono ma non sono limitate a tubercolosi, malaria, linfoma, lupus, malattia di Lyme, infezioni virali, malattie del tessuto connettivo, uso di droghe IV e gravidanza.
– L’enzima di conversione dell’angiotensina (ACE) supporta una diagnosi di sarcoidosi e aiuta a monitorare l’attività della malattia durante il trattamento. Un test del lisozima nel siero può anche essere usato per verificare la sarcoidosi.
– La radiografia del torace (CXR) o la tomografia computerizzata (CT) è anche utile quando si indaga per la tubercolosi o i noduli sarcoidi nei polmoni.6 Normalmente, quando ordino una CXR per escludere la sarcoidosi, richiedo immagini posteriori-anteriori e laterali (PA/LAT). In ogni caso, è importante annotare ciò che si sta cercando (ad esempio, escludere i noduli sarcoidi in presenza di un’uveite bilaterale) per aiutare il radiologo a orientarsi nel suo esame. In un ambiente ospedaliero, è anche fondamentale, quando si ordinano questi test, coinvolgere il medico di base del paziente (PCP) o lo specialista appropriato se si trovano anomalie.
Per gli oculisti che non hanno accesso ai laboratori o alla diagnostica per immagini, inviare il paziente al suo medico di base con le raccomandazioni esatte di quali test ordinare e perché aiuterà il paziente in modo rapido e aiuterà a guidare il medico di base che si affida alla vostra esperienza per le condizioni oftalmiche.
– L’antigene leucocitario umano B27 (HLA-B27) si trova sulla superficie dei globuli bianchi ed è associato a una serie di disturbi autoimmuni, come la spondilite anchilosante e la sindrome di Reiter. Tuttavia, non è necessariamente un marcatore specifico per qualsiasi malattia, e può effettivamente essere il singolo fattore determinante in alcuni casi di irite.4
– Test del derivato proteico purificato (PPD) per la tubercolosi latente.
– Lyme titolo e saggio di immunoassorbimento enzimatico (ELISA), insieme con anti-Borrelia burgdorferi immunoglobuline M e G (IgM / IgG), sono utilizzati per rilevare la presenza della malattia di Lyme. L’ELISA può anche essere usato per rilevare l’HIV, così come il test Western Blot.2,7
Altri test non comuni per l’uveite che possono avere rilevanza in alcune presentazioni di pazienti includono un profilo di anticorpi di Sjögren (SS-A, SS-B), analisi delle urine e una ricerca di entità virali come anticorpi IgG/IgM del citomegalovirus (CMV). Ricordiamo dall’immunologia che le IgG rappresentano l’esposizione passata o l’immunità a una malattia, e le IgM rappresentano l’esposizione recente o una probabile infezione attiva.
Gestione dell’Uveite non traumatica
I primi episodi di irite lieve e unilaterale sono spesso idiopatici e associati a un’infezione virale o sinusale, o a un evento traumatico. Ulteriori test diagnostici di solito possono essere evitati, perché l’osservazione e il trattamento dei sintomi sono in genere sufficienti in questi casi a basso rischio.2 A seconda della gravità dell’infiammazione in un caso di irite traumatica, i farmaci antinfiammatori a volte possono essere trattenuti. Tuttavia, un sano giudizio clinico deve essere esercitato quando si determina se e quando l’uso di farmaci è necessario.
Per qualsiasi sforzo terapeutico, un obiettivo di trattamento specifico è fondamentale. Ovviamente, aumentare il comfort del paziente è fondamentale nella cura dell’uveite. Lo scopo fondamentale nella gestione dell’uveite si impernia sulla riduzione dell’infiammazione, diminuendo così la morbilità e la probabilità di altre complicazioni più gravi, come la perdita della vista e il glaucoma.
Alla luce di questi obiettivi, quattro obiettivi principali dovrebbero essere considerati quando si tratta un paziente affetto da irite:
– Diminuire il dolore.
– Prevenire le sinechie posteriori e quindi il blocco pupillare.
– Prevenire le sinechie anteriori periferiche (PAS) e quindi la chiusura degli angoli.
– Ristabilire la barriera emato-acquosa.
L’tropina e altri cicloplegici/midriatici simili svolgono un ruolo integrale in tutti e quattro gli obiettivi.4 Gli agenti cicloplegici agiscono sulla vascolarizzazione per aiutare a stabilizzare la barriera emato-acquosa, impedendo ulteriori perdite. Immobilizzando l’iride, insieme alla loro azione nella paresi dei muscoli ciliari, i cicloplegici non solo aiutano nel controllo del dolore, ma il loro effetto dilatante è altrettanto importante nel contrastare la chiusura dell’angolo e il blocco pupillare evitando l’adesione dell’iride alla lente. I corticosteroidi (di solito topici nella maggior parte dei casi di uveite anteriore) riducono la risposta infiammatoria del corpo e sono un pilastro nella cura dell’irite. Aiutano anche a ridurre la permeabilità capillare e la vasodilatazione.4,7,13
Altre opzioni terapeutiche includono farmaci antinfiammatori non steroidei (FANS), agenti immunosoppressivi/immunomodulatori e opzioni chirurgiche (per esempio, iridotomia periferica laser o impianto perioculare).2,3,9,12 L’uso di corticosteroidi nell’uveite normalmente deve essere ridotto per evitare un’infiammazione di rimbalzo.
Somministrazione precoce e frequente di steroidi è classicamente prescritta per garantire una dose di carico adeguata al fine di sedare aggressivamente l’infiammazione. La rastremazione appropriata, secondo la risposta clinica, assicura la corretta remissione dell’uveite senza un rimbalzo dell’infiammazione.3 Tuttavia, se uno steroide viene prescritto nell’uveite traumatica, è generalmente per un breve periodo di tempo, eliminando la necessità della rastremazione dei farmaci – soprattutto perché lo stimolo infiammatorio (trauma) è scomparso.
L’aumento della IOP e la cataratta subcapsulare posteriore (PSC) sono due preoccupazioni primarie associate all’uso di corticosteroidi; tuttavia, queste complicazioni non sono viste di routine dopo un uso a breve termine. Allo stesso modo, l’aumento della PIO con l’uso concomitante di corticosteroidi non significa sempre che lo steroide sia la causa dell’aumento. Nell’uveite, la IOP è generalmente più bassa del normale – anche se in alcuni casi può essere più alta del normale, a seconda del momento del processo della malattia in cui il paziente si presenta per le cure.1,4,11 Due possibili ragioni per la diminuzione della IOP includono:1,4
– Un aumento del rilascio di prostaglandine endogene aumenta il deflusso uveosclerale.
– Una diminuzione della produzione di umor acqueo dal corpo ciliare infiammato.1,4
Le spiegazioni potenziali dell’aumento della PIO includono:
– L’intasamento della rete trabecolare con cellule infiammatorie e proteine.
– La trabeculite, o fibre della rete infiammate e gonfie.
– Le sinechie posteriori.
– Le sinechie anteriori periferiche.
– Innalzamento della IOP indotto da steroidi.
– Il fatto che l’occhio “malato” stia tornando alla normalità.
Un aumento della IOP può verificarsi durante il periodo di trattamento con corticosteroidi, ma non è sempre secondario agli effetti collaterali del corticosteroide stesso. Pertanto, il termine “risponditore agli steroidi” è talvolta erroneamente attribuito alla normalizzazione della produzione di acquosa da parte dell’occhio in via di guarigione prima che il reticolo trabecolare abbia completamente fagocitato i globuli bianchi e i resti di proteine fibrinose dall’angolo di drenaggio.4 Interrompere prematuramente il trattamento steroideo prima della completa risoluzione infiammatoria può, infatti, fare più male che bene; invece, il trattamento steroideo dovrebbe essere mantenuto e dovrebbe essere aggiunto un farmaco per l’abbassamento della IOP (cioè, un soppressore acquoso), come un beta-bloccante o un inibitore dell’anidrasi carbonica.
È importante notare che gli analoghi delle prostaglandine e i miotici devono essere evitati nell’uveite, perché possono aumentare l’infiammazione.8,10-12 I miotici aumentano anche il rischio di formazione di sinechie posteriori.1 Gli agonisti adrenergici, come la brimonidina e l’apraclonidina, sono generalmente sicuri da usare nei pazienti con uveite con aumento della PIO.
Quando si tratta di uveite anteriore, l’esatto schema di dosaggio è più arte che scienza, poiché ogni caso può presentarsi in modo diverso e strategie leggermente sfumate possono produrre risultati positivi simili. Un tipico protocollo di trattamento comprende la somministrazione di una goccia di prednisolone acetato 1,0% ogni ora per due o tre giorni, o fino a quando si vedono cellule lievi (< grado 2). Poi, la riduzione pianificata dello steroide può essere realizzata tagliando continuamente la frequenza di somministrazione a metà ogni terzo giorno.
Per presentazioni più lievi, loteprednol etabonato gel 0,5% somministrato con un programma di dosaggio meno frequente potrebbe essere meglio. Per i casi più gravi o recalcitranti, tuttavia, l’emulsione oftalmica difluprednate 0,05% QID o Q2H può essere appropriata. Alcuni pazienti possono anche richiedere corticosteroidi orali; una scelta comune è il prednisone, che di solito è dosato tra 20 mg e 40 mg con una frequenza da BID a QID per diversi giorni. Quando si prescrivono corticosteroidi orali, prendere nota di eventuali malattie sistemiche, così come altri farmaci che il paziente sta usando, in caso di effetti collaterali o interazioni tra i diversi farmaci.
Come tale, si consiglia di consultare il PCP del paziente prima di prescrivere corticosteroidi orali. Si dovrebbe anche considerare la possibilità di prescrivere un antistaminico che agisce per inibire la produzione di acido gastrico, come la ranitidina (Zantac, GlaxoSmithKline), al fine di prevenire disturbi gastrointestinali. Come minimo, assicurarsi che il paziente prenda il corticosteroide orale con del cibo o del latte.
Come già detto, i cicloplegici, come l’omatropina 5,0% o l’atropina 1,0%, sono necessari per una corretta gestione dell’uveite. Un approccio comune può includere una goccia di omatropina 5% TID per tre giorni, BID per due giorni e QD per un giorno; tuttavia, un periodo prolungato di diverse settimane può essere necessario per i casi più gravi. Ricordate, perché l’occhio è infiammato, una strategia di dosaggio che è maggiore dell’emivita del farmaco sarà necessaria. Questo perché il farmaco viene metabolizzato a un ritmo molto più veloce in un occhio malato. A seconda della gravità, il paziente deve tornare per una visita di controllo inizialmente tra due e cinque giorni, poi secondo necessità.
Gestione dell’uveite traumatica
La frequenza dell’uveite negli Stati Uniti corrisponde alle cifre internazionali con circa 15 casi ogni 100.000 persone.6,7 Il trauma è la terza causa più comune di uveite anteriore.6,7 La morbilità deriva generalmente da sintomi, sinechie posteriori, edema maculare cistoide, aumento della IOP con conseguente glaucoma, formazione di cataratta e retinopatia.4,6,9 Altre complicazioni associate all’irite traumatica includono ipema, iridodialisi, iridoschisi, dislocazione e/o opacizzazione del cristallino, commotio retinae, neuropatia ottica, distacco posteriore del vitreo, lacerazioni e distacchi della retina, rottura della coroide, edema corneale e recessione angolare.5,9-11
L’ipema, se presente, è una condizione grave che richiede un attento monitoraggio. I pazienti sono tipicamente confinati al riposo a letto con attività limitata, dove la loro testa dovrebbe essere sollevata di almeno 30° e uno schermo posto sopra l’occhio per una maggiore protezione. I pazienti dovrebbero evitare l’aspirina, ma possono prendere acetaminofene per il dolore, se necessario.
Atropina 1.0% dovrebbe essere in-stillata da QD a TID e prednisolone acetato 1.0% dosato da Q2H a QID. L’acido aminocaproico orale, un antifibrinolitico, dovrebbe anche essere somministrato, a seconda della dimensione dell’ipema.10-12
Anche gli studi di laboratorio dovrebbero essere considerati per i casi di ipema. Le analisi tipiche ordinate includono l’emocromo completo (CBC) con differenziale, tempo di protrombina (PT), tempo di tromboplastina parziale (PTT), azoto ureico nel sangue (BUN), creatinina, elettroliti, studi di falcemia ed emoglobina. Anche i farmaci per la IOP (cioè i beta-bloccanti) dovrebbero essere istituiti se la IOP è elevata in modo significativo. Le prostaglandine e i miotici dovrebbero essere evitati, perché possono aggiungersi all’effetto infiammatorio.8,10-12
La recessione angolare si nota se c’è un’inserzione posteriore dell’iride irregolare, che permette di vedere una banda del corpo ciliare più grande del normale.8 Questo può essere confermato se i risultati gonioscopici dell’occhio controlaterale sono normali. La recessione dell’angolo non si verifica sempre con un trauma contundente e, se presente, non sempre produce un’elevata IOP all’inizio. Tuttavia, il danno microscopico alle cellule endoteliali del reticolo trabecolare è possibile, con conseguente aumento della PIO anni dopo il trauma iniziale.8,10 Sono necessari esami oculistici regolari per monitorare questi pazienti per complicazioni future.
L’uveite può presentarsi contemporaneamente ad altre patologie. Pertanto, è prudente essere scrupolosi quando si esamina un paziente con infiammazione del segmento anteriore. Un’anamnesi metodica spesso può individuare la causa dell’infiammazione. Inoltre, sapere cosa cercare durante la valutazione con la lampada a fessura è imperativo, in modo che una gestione adeguata e ulteriori test diagnostici, se necessario, possano essere istituiti in modo rapido.
L’irite può variare da lieve a grave, con perdita della vista e persino cecità se non trattata. La maggior parte dei casi di irite che si presentano al primario sono localizzati anteriormente, di gravità da lieve a moderata e relativamente semplici da gestire. La prognosi è generalmente favorevole con un trattamento appropriato e regimi di follow-up; i pilastri per una corretta gestione rimangono i corticosteroidi e i cicloplegici. I casi bilaterali e ricorrenti possono richiedere ulteriori indagini sull’eziologia. Nel complesso, è fondamentale educare i pazienti sui sintomi e sull’importanza dei futuri esami oculistici periodici per monitorare le complicazioni.
Il dottor Dohm è il capo del dipartimento di optometria e il direttore associato per i servizi medici al Naval Hospital Oak Harbor sulla Naval Air Station Whidbey Island a Oak Harbor, Wash. Non ha interessi finanziari diretti in nessuno dei prodotti menzionati.
1. Yanoff M, Duker JS (eds.). Oftalmologia, 2a ed. St. Louis: Mosby; 2004.
2. Medscape. Classificazione dell’uveite. Disponibile presso: http://emedicine.medscape.com/article/1208936-overview. Accesso 8 novembre 2012.
3. Smith RE, Nozik RM. Uveite: Un approccio clinico alla diagnosi e alla gestione. Baltimora: Williams & Wilkins; 1983.
4. Harkins TJ. Comunicazione personale. Kansas City Veterans Administration Medical Center; Kansas City, MO. Agosto-dicembre 2005.
5. Oro DH. Atlante clinico dell’occhio. Chicago: AMA Press; 2002.
6. Medscape. Iritis e Uveite. Disponibile a: http://emedicine.medscape.com/article/798323-overview. Acceduto il 10 novembre 2012.
7. Medscape. Valutazione e trattamento dell’uveite. Disponibile a: http://emedicine.medscape.com/article/1209123-overview. Accessed November 10, 2012.
8. Kunimoto DY. Il manuale dell’occhio di Wills: Office and Emergency Room Diagnosis and Treatment of Eye Disease, 4th ed. Filadelfia: Lippincott Williams & Wilkins; 2004.
9. Kanski JJ. Oftalmologia clinica: A Systematic Approach. 5a ed. Londra: Butterworth Heinemann; 2003.
10. Shingleton BJ, Hersh PS, Kenyon KR (eds.). Trauma oculare. St. Louis: Mosby; 1991.
11. Keil J, Chen S. Lesioni da contusione e loro effetti oculari. Clin Exp Optom 2001;84(1):19-25.
12. Kaiser PK, Friedman NJ, Pineda R. The Massachusetts Eye and Ear Infirmary Illustrated Manual of Ophthalmology, 2nd ed. Filadelfia: Saunders; 2004.
13. Pavan-Langston D. Manuale di diagnosi e terapia oculare, 4 ° ed. Boston: Little, Brown and Company; 1996.
.