Kolonoskopi för screening av tjocktarmscancer är effektivt för att både minska dödligheten genom tidig upptäckt och förebygga genom avlägsnande av precancerösa polyper (1-8). Dessa fördelar kan dock motverkas av bristande kvalitet på koloskopin och komplikationer (9-17). Missade polyper och ofullständig polypektomi kan bidra till utveckling av intervallcancer (cancer som upptäcks efter koloskopi) (10-14, 18, 19). Även om blödning efter koloskopi är relativt ovanlig, den förekommer hos 1-6/1000, (15-17) är den den främsta komplikationen som leder till oplanerade sjukhusbesök inom 7 dagar efter koloskopi (20). Polypektomi är den överväldigande orsaken (21-26). Riskfaktorer som ökar blödningen efter polypektomi är bland annat polypsstorlek, antal polyper, antikoagulationsbehandling och polyphistologi (17, 21, 27, 28). Avancerade polypektomitekniker som endoskopisk mucosal resektion (EMR) och endoskopisk submucosal dissektion (ESD) tycks mer fullständigt avlägsna polyper, men ökar också procedurtiden, kostnaden och blödningsriskerna (17, 29-31).
Bortsett från EMR och ESD har liten uppmärksamhet ägnats åt polypektomiteknik som en riskfaktor för blödning efter polypektomi. Den allmänt accepterade och allmänt använda traditionella snara-polypektomitekniken för att giljotinera den fasthållna polypen med eller utan värmekoagulering har faktiskt inte förändrats mycket på nästan fem decennier (32-37). För att förhindra blödning efter polypektomi utvecklade en av författarna (ZJC) endoskopisk mucosal stripping (EMS) som en modifiering av traditionell cold snare-polypektomi (TCSP) för att undvika att skära in i blodkärlsrik submucosa, eftersom alla icke-cancerösa polyper, som är den vanligaste typen av polyper som ses vid screeningkoloskopi, per definition är begränsade till mukosa och inte sträcker sig in i submucosa. Den 31 december 2012 fattades ett beslut om att systematiskt anta den tekniska innovationen eftersom EMS tidigt visade sig vara framgångsrik när det gällde att fullständigt avlägsna icke-pedunkulerade polyper utan betydande skador på submucosan. Denna rapport analyserade effektiviteten av EMS för att förhindra blödning efter polypektomi och underlätta fullständig polypborttagning, särskilt för avancerade polyper med hög risk.
- Metoder
- Patienter och studiedesign
- Endoskopisk slemhinnestrippning (EMS)
- Outcome Assessment
- Koloskopiundersökning
- Statistisk analys
- Resultat
- EMS förhindrade sjukhusvårdskrävande blödningar efter polypektomi
- EMS underlättade fullständig polypektomi
- Diskussion
- Etiskt uttalande
- Författarbidrag
- Intressekonfliktförklaring
- Acknowledgments
- Supplementary Material
- Abkortningar
Metoder
Patienter och studiedesign
Detta var en retrospektiv undersökning av data som införlivade elektroniska medicinska journaler och patologislides vid Minnesota Gastroenterology, PA (MNGI). Ett undantag från den interna granskningsnämnden beviljades för undersökningen. Patienterna var de som fick koloskopi med snare-polypektomi enligt Current Procedural Terminology (CPT) kod 45385 av ZJC på MNGI ambulatoriska endoskopicenter under en 12-årsperiod uppdelad i pre-EMS-eran (2005-2012) och EMS-eran (2013-2016). En databassökning utfördes för fall av blödning efter polypektomi som krävde sjukhusvistelse och avancerade polyper definierade som polyper med villösa drag, höggradig dysplasi, sessila serrerade adenom med cytologisk dysplasi (SSACD) samt alla adenomatösa polyper 10 mm eller större. Eftersom MNGI hade en omfattande lokal praktikertäckning och en dygnet runt bemannad telefonlinje för komplikationer hade man en nästan fullständig fångstfrekvens för komplikationer som granskades av kollegor och återkopplades till de inblandade endoskopisterna för kvalitetsförbättring.
Endoskopisk slemhinnestrippning (EMS)
Endoskopisk slemhinnestrippning (EMS) är ett endoskopiskt avlägsnande av polypinnehållande slemhinna genom mekanisk strippning med hjälp av en kall snara. Det är en modifiering av TCSP i och med att EMS avlägsnar slemhinnan från den fastspända submucosan vid det potentiella utrymmet mellan dem (figur 1, kompletterande video) i stället för att giljotinera hela den fastspända vävnaden som ursprungligen beskrevs för TCSP (36, 37). EMS förväntas därför minimera submucosal skada och tillhörande omedelbar och fördröjd blödning. För den sällsynta pedunkulerade polypen använder vi fortfarande hot snare-polypektomi eftersom den cautery-inducerade vävnadsskadan till stor del kan begränsas till den intraluminala stjälken och inte sträcker sig djupt in i kolonväggen. Därför tillämpade vi EMS uteslutande på icke-pedunkulerade polyper utan tecken på malignitet. Nedan beskriver vi detaljerna i EMS-teknikerna baserat på polypernas storlek.
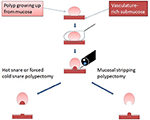
Figur 1. Diagram som illustrerar den kritiska skillnaden mellan EMS och traditionell snare-polypektomi. Återges från Chen och Batts (38), Copyright (2017) med tillstånd från Elsevier för användning som open access-innehåll under CC-BY-användarlicens.
För små polyper (≤ 5 mm) fungerar TCSP i allmänhet bra. För att säkerställa fullständig resektion föredrar vi snara framför biopsitång utom för diminutiva polyper 2 mm eller mindre (25) och tar rutinmässigt bort 2-3 mm intilliggande mukosa under polypektomi. Submucosa kan dock fortfarande fastna inuti snaren, vilket förhindrar fullständig stängning av snaren utan giljotin med brutal kraft eller värmekoagulering (hot snare). När detta inträffar leder en stadig och försiktig dragning av snarren in i skopet samtidigt som snarren hålls stadigt men inte tätt stängd vanligtvis till att den polypinnehållande slemhinnan avskalas/nålas bort och lämnar kvar den instängda submucosan som bildar en övergående upphöjd pseudostjälk (figur 2A). Endoskopiskt sett är den avrivna slemhinnan vanligtvis i ett stycke medan submucosan förblir i stort sett intakt utan blodkärlsskador (figur 2B). Den slemhinnebristning som orsakas av EMS skapar i allmänhet ett polypektomiplats som är något större men mycket mindre blodigt än vad som skulle orsakas av TCSP. För att EMS ska vara effektivt är det viktigt att hålla snaran fast men inte för hårt stängd under strippningen. Om snaran inte stängs tillräckligt hårt kan det leda till att snaran glider, medan om den stängs för hårt kan det leda till submukosal skada, t.ex. hematombildning och misslyckad strippning. En erfaren endoskopist kan lätt känna av subtiliteten och instruera den assisterande endoskopisjuksköterskan att justera lämplig fasthet i greppet när man drar i snaran.
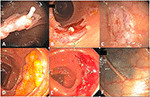
Figur 2. EMS-polypektomier. (A) Submucosal pseudostalk efter polypektomi av ett 10 mm sessilt tubulärt adenom i cecal. (B) En intakt bit polypinnehållande mukosa efter avlägsnande (övre höger) och den polypfria polypfria polypektomiplatsen med synlig pseudostalk (nedre vänster). (C) En ren polypektomiplats utan deformitet trots mindre övergående kapillär ozonering omedelbart efter polypektomi. Lyftning av den instängda slemhinnan förhindrade utvecklingen av pseudostalken. (D) Ett 30 mm tjockt, sätesfritt, serrerat adenom i tvärkolon. (E) Polypektomiplatsen i (D) efter piecemeal polypektomi. (F) Samma tatuerade polypektomiplats som (E) 1 år senare.
Medan submucosal entrapment kan undvikas för mindre polyper genom att placera snaran optimalt och försiktigt lyfta polypen, kan detta bli oundvikligt vid avlägsnande av större polyper. Även om den ovan beskrivna tekniken fortfarande är tillämplig, förhindrar den fasthållna submucosan ofta att snara separeras från polyputtagningsstället även efter det att den polypinnehållande slemhinnan redan har avlägsnats. Under sådana omständigheter finns det ingen anledning att ytterligare dra ut snärjan med brutalt våld. Genom att öppna snaran något och föra den över den fasthållna submucosan frigörs snaran och eventuell borttagen men fortfarande till synes fastsatt polypinnehållande slemhinna från polypektomiplatsen. Den inbundna submucosan från dessa större polyper bildar ofta en tjockare pseudostjälk men submucosal skada förblir minimal.
För ännu större polyper som inte kan avlägsnas i ett stycke kan EMS piecemeal polypektomi utföras. Eftersom EMS brist på submucosal skada skapar en mindre blodig eller deformerad polypektomiplats i jämförelse med traditionell kall eller varm snara-polypektomi, visualiseras eventuell kvarvarande polyppvävnad bättre vilket underlättar fullständig polypborttagning (Figur 2).
Outcome Assessment
1. Blödningsfrekvenser efter polypektomi som kräver sjukhusvistelse för alla och icke-pedunkulerade kolonpolyper före och efter EMS-användning.
2. Fullständighet av EMS-polypborttagning fastställd genom biopsi på polypektomiplatsen och undersökning under uppföljande koloskopi med de intervall som rekommenderas i nationella samhällsriktlinjer (13, 14).
Koloskopiundersökning
Koloskopier utfördes med hjälp av koloskop med variabel styvhet (PCF 160, CF 160, PCF 180 och CF 180; Olympus Corp. Tokyo, Japan) i de flesta fall och FUSE-koloskop med fullt spektrum (EndoChoice, Alpharetta, Georgia) i några få fall som en del av ett försök. Polypektomier utfördes huvudsakligen med hjälp av ovala snaror (100600 till 100602, ConMed, Utica, NY) och, i några få fall, spiralsnara (SD-230U-20, Olympus Corp, Tokyo, Japan) och Exacto-snara (BX00711115, US Endoscopy, Mentor, OH).
Som en del av MNGI:s kvalitetsmätning rapporterades följande årliga koloskopistatistik för ZJC för 2014 och 2016: räckvidd för blindtarmen 99,5-100 %, upptäckt av adenomatösa polyper vid screeningkoloskopi 50,3-60,1 % för män och 42.1-54,0 % för kvinnor.
Statistisk analys
Den statistiska analysen utfördes med hjälp av Fishers exakta test.
Resultat
EMS förhindrade sjukhusvårdskrävande blödningar efter polypektomi
Totalt 5 142 koloskopier med snare-polypektomi som utfördes av ZJC vid MNGI:s ambulerande endoskopicentra under 12 år delades upp i pre-EMS-eran (2005-2012, n=2 973) och EMS-eran (2013-2016, n=2169) (tabell 1). Den sista sjukhusvårdskrävande blödningen efter polypektomi inträffade i september 2012. Ingen hittades under EMS-eran (frekvens 0 %) medan tio (inklusive 2 pedunkulerade polyper) hittades under pre-EMS-eran (frekvens 0,336 %). Inläggning på sjukhus skedde 1-16 dagar efter koloskopier. Denna skillnad var statistiskt signifikant (P = 0,0055) och förblev så efter att ha uteslutit de 2 fallen av pedunkulerade polyper (P = 0,012).
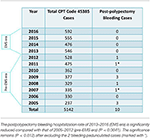
Tabell 1. Fall av blödning efter polypektomi och fall av total snare-polypektomi (CPT-kod #45385) under 12 år.
Av de 12 blödningsfallen avlägsnades totalt 18 polyper. Med undantag för två 2-3 mm tubulära adenom (TA) som avlägsnades med en kall snare, avlägsnades alla med en varm snare. Dessa inkluderade tio 8-40 mm TA (inklusive två pedunkulerade polyper på 11-15 mm respektive 36-40 mm), ett 25 mm tubulovillöst adenom (TVA), fyra 6-10 mm sessila serrerade adenom (SSA) och ett 5 mm lipom. Med undantag för ett fall som endast hade en partiell återvinning av den resecerade polypen och som mikroskopiskt sett inte hade någon submucosa, visade alla övriga nio fall tecken på cauteriserad submucosa, ofta med synliga blodkärl nära den cauteriserade kanten, vilket illustreras i figur 3C. Dessa fynd tyder på att submucosal skada under hot snare polypektomi bidrog till blödning efter polypektomi.
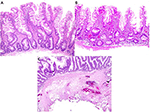
Figur 3. Histopatologisk jämförelse av avancerade polyper som avlägsnats med EMS och hot snare-polypektomi. (A,B) Polyper som avlägsnas med EMS visar vanligtvis en djup aspekt av muscularis mucosae med en sparsam submucosa och avsaknad av blodkärl. (C) Låg förstoring av en polyp som avlägsnats med hjälp av hot snare visar typisk mängd submucosa med vävnadsskada orsakad av cautery.
För att göra en jämförelse undersökte vi också mikroskopiskt 20 på varandra följande fall av avancerade kolonpolyper som avlägsnats med hjälp av EMS. Dessa polyper innehöll endast varierande mängd muscularis mucosae och sparsam, om ens någon, submucosa utan blodkärl (tabell 2, figur 3A,B). Dessa resultat tyder på att EMS förhindrade blödning efter polypektomi genom att undvika skador på submucosan.
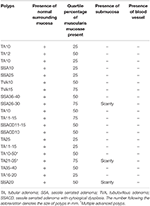
Tabell 2. Egenskaper hos 20 konsekutiva fall av avancerade kolonpolyper som avlägsnats med hjälp av EMS.
EMS underlättade fullständig polypektomi
Extensiva biopsier utfördes på kanten (x4) och pseudostängeln (x1) av 10 slumpmässigt utvalda avancerade polypställen efter endoskopiskt fullständig avlägsnande med hjälp av EMS. Inga polyprester hittades i något prov. Nittiosju neoplastiska EMS-polypektomiområden följdes från 6 månader till 4 år, inklusive 38 polypektomiområden hos 23 patienter efter avlägsnande av avancerade polyper. Ingen av de 59 icke-avancerade neoplastiska polyperna (< 10 mm och utan avancerade egenskaper) hade några kvarvarande eller återkommande polyper vid uppföljande koloskopi. Den stora majoriteten (33 av 38; 87 %) av de avancerade polypställena hade inte heller några polyper vid uppföljande koloskopi (tabell 3). Två små polyper hittades nära polyp #12 platsen 1 år senare men var av en annan typ än den ursprungliga (SSA vs. TA). För polyperna #13, #22 och #25 hittades visserligen vid uppföljande koloskopier 1-3,5 år senare en liten (2-5 mm) polyp av samma typ (TA) nära den ursprungliga polypektomiplatsen i varje fall, men det var svårt att avgöra om polyperna var nybildade eller rester eftersom de alla förekom i polyposfall med 24, 10 respektive 14 adenomatösa polyper som avlägsnats vid de kombinerade inledande och uppföljande koloskopierna. Olika typer av små polyper (SSA snarare än TA) upptäcktes också i närheten av de ursprungliga polypskirurgiska platserna för polyp nr 13 och 25 vid den uppföljande koloskopin, vilket ytterligare tyder på att det rörde sig om ny polyptillväxt snarare än ofullständig polypskirurgi. En 10 mm stor SSA hittades 14 månader senare bakom ett veck nära den tatuerade polypektomiplatsen för den 50 mm stora platta SSA:n (nr 26). Detta skulle kunna vara en inkomplett polypektomi, möjligen på grund av den ursprungliga polypens extra stora storlek, men det skulle också kunna vara en växande separat polyp som missades vid den ursprungliga koloskopin på grund av dess mycket dolda läge bakom ett veck som bäst syns vid retroflexion (figur 4). Således fanns det inte ett enda övertygande fall och högst 4/97 (4,1 %) av alla följda neoplastiska polyper eller 4/38 (10,5 %) av de avancerade polyper som avlägsnats med hjälp av EMS hade ofullständig polypektomi. Dessa siffror jämfördes mycket gynnsamt med dem som rapporterats för traditionella snara-polypektomitekniker (18).
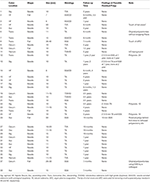
Tabell 3. Uppföljning av 38 avancerade kolonpolyper som avlägsnats med EMS hos 23 patienter.
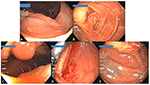
Figur 4. (A) Ett stort 50 mm stort sessilt serrerat adenom (Polyp nr 26 i tabell 3) i proximala ascenderande kolon med ICV synlig i bakgrunden (pil). (B) Översikt över polypektomiplatsen 14 månader senare med en av tatueringarna synlig till höger (pilar). (C) En 10 mm SSA dold bakom ett veck (pilar) nära polypektomiplatsen. (D) Polypectomiplatsen för polypen i (C) på retroflexionsvyn. (E) Relativt utrymme för en av tatueringarna (vänster nedre) och det veck bakom vilket polypen i (C) gömde sig (pil).
Diskussion
Våra dataanalyser bekräftar att EMS förhindrade blödning efter polypektomi och underlättade fullständigt avlägsnande av polypen jämfört med traditionella snara-polypektomitekniker. EMS skulle därför kunna göra koloskopi säkrare och effektivare som ett verktyg för att förebygga tjocktarmscancer.
Koloskopikomplikationer som blödning efter polypektomi och perforation uppstår på grund av skador på submucosa och djupare vävnader. Sådana skador är inte nödvändiga vid avlägsnande av precancerösa kolonpolyper och bör undvikas.
Submucosa är rik på bindväv och blodkärl. Den fastnar ofta under snare-polypektomi och förhindrar fullständig stängning av snare utan brutal giljotin eller värmekoagulering. TCSP-tekniken för att giljotinera hela den fastspända vävnaden skadar den fastspända submucosan, även om det sker i mindre utsträckning jämfört med hot snare-tekniken (39). Den ökade omedelbara blödningsfrekvensen med TCSP som kräver hemostatiska ingrepp, t.ex. klippning, kan inte bara försämra upptäckten av polyprester utan begränsar också dess tillämpning på större polyper (39-42). Genom att undvika att skära submucosan helt och hållet förhindrar EMS omedelbar och fördröjd blödning och verkar säker för större polyper även utan att stoppa antikoagulation och trombocythämmande behandlingar (figur 5).

Figur 5. (A) Ett 15 mm stort transsektionellt colon sessilt serrerat adenom med cytologisk dysplasi (Polyp#7 i tabell 3). (B) Polypektomiplatsen omedelbart efter avlägsnande av polypen i (A). (C) Samma polypektomiplats som i (B) 6 månader senare. Den här patienten slutade inte med klopidogrel vid tiden för polypektomi. Med EMS säkerhetsprofil fattades ett beslut om att fortsätta med polypektomi med tanke på att hon kunde få en svår upprepad koloskopi på grund av sin höga ålder (4 månader före 80 års ålder) och en lång och slingrig tjocktarm med förstoppning. Hon fick så småningom en koloskopi 6 månader senare för polypens högriskhistopatologi.
Ett potentiellt bekymmer är EMS-polypektomins fullständighet, särskilt i pseudostalken. Våra biopsiuppgifter från polypställe och andras analys av pseudostalken efter kallsnara-polypektomi (43) visade att polypen avlägsnades fullständigt. Detta stöds ytterligare av den frekvens med vilken vi upptäckte möjliga kvarvarande polyper vid EMS-polypektomiställen under uppföljande koloskopi (sannolikt 0 % och högst 4,1 % alla neoplastiska eller 10,5 % avancerade polyper), vilket är mycket lägre än vad som tidigare rapporterats (18). Baserat på provtagningar av kanterna på de endoskopiskt ”kompletta” polypektomierna noterade Pohl et al oväntat persisterande neoplasmer i 10,1 % av alla polypektomier, 17,3 % av 10-20 mm neoplastiska polyper, större andelar för SSA än för TA (31 jämfört med 7,2 %), och 47,6 % av alla stora (10-20 mm) SSA avlägsnades ofullständigt (18). Zhang et al. rapporterade på liknande sätt ofullständig TCSP av polyper (6-9 mm) (8,5 % i genomsnitt och 13 % för piecemeal resektion) med omedelbar blödning som krävde klippning förekom i 1,8 respektive 2,7 % per polyper och per patient (40). En trolig förklaring till skillnaden är att EMS-polypektomiplatserna var mindre traumatiska med minimal blödning eller deformation jämfört med dem vid traditionell kall eller varm snare-polypektomi. Detta underlättade inte bara upptäckten och avlägsnandet av polyperrester utan möjliggjorde också en mer generös slemhinneresektion utan oro för blödning och andra komplikationer. Fullständig polypektomi är viktig för att förebygga intervallkoloncancer som står för 2,6-9,0 % av den totala koloncancernsfrekvensen (19).
Pedunkulerade polyper kan ha en hög risk för blödning efter polypektomi eftersom submucosal skada är oundviklig. Erfarenhetsvinster kan ha lett till minskad blödning från dessa sällsynta polyper eftersom ZJC flyttade snittet bort från tjocktarmsväggen och nära polypen på stjälken. Men minskningen av blödningen efter polypektomi från stubbiga polyper före och efter EMS var inte statistiskt signifikant. Vi tror att EMS snarare än erfarenhetsvinster ledde till eliminering av postpolypectomiblödning från icke-pedunkulerade polyper.
Ett hematom kunde sällan utvecklas från ett rivet submucosalt kärl under EMS av stora polyper. Den intakta submucosan hindrar dock ett eventuellt hematom från att förstoras och förblöda. Enligt vår erfarenhet verkade den naturliga barriär som tillhandahålls av intakt submucosa vara överlägsen den koagulering som tillhandahålls av varm snara när det gäller att förhindra fördröjd blödning efter polypektomi.
Vid jämförelse med EMR är EMS mycket lättare att utföra och kan uppnå samma polypektomiresultat även för vissa stora lateralt utbredda lesioner (tabell 3) utan ytterligare resurser och med mycket minskad blödningsrisk. Ytterligare studier behövs för att direkt jämföra EMS och EMR, särskilt vid avlägsnande av stora polyper.
Då EMS endast avlägsnar slemhinnan, ligger eventuell tidig cancer med submucosal invasion utanför dess räckvidd. Noterbart är att vi under studieperioden stötte på ett fall av en 10 mm oanmäld cancer i kolonets sessila polyp som inte var misstänkt för cancer. Intressant nog fortsatte polypektomiplatsen att sippra och krävde hemoklippning. Diagnosen erhölls först efter polypborttagning och patienten hänvisades därefter till kirurgi utan incidens. Förstorad gropmönsterdiagnostik kan ha varit till hjälp vid en prediagnostik i detta fall och noggrann undersökning av polypen uppmuntras alltid före EMS för att undvika att skära upp cancerpolyper. Inget negativt utfall inträffade dock i detta fall.
EMS kan utföras med spiral- eller Exacto-snaror och i kombination med submucosal injektion för att lyfta slemhinnan, argonplasmakoagulering eller ablation med heta snarspetsar. Det återstår att se om de ytterligare förbättrar EMS-effekten.
EMS har framgångsrikt införts av en hel del MNGI-kollegor (tabell 3, #37-38) men generaliserbarheten av dess fördelar behöver ytterligare bekräftande studier. Icke desto mindre kan denna relativt enkla men effektiva innovation i polypektomitekniken utgöra en ny gräns för säkrare och effektivare koloncancerprevention genom koloskopi.
Etiskt uttalande
Denna retrospektiva studie beviljades undantag från IRB Review Determination den 12 maj 2016 (IRB ID: 5502) av Sterling IRB (www.sterlingirb.com) och genomfördes i enlighet med det godkända protokollet Clinical and Histopathological Review of Mucosal Stripping as a Colonoscopy Polypectomy Technical Innovation och rekommendationerna från Minnesota Gastroenterology Quality Committee. Alla försökspersoner gav skriftligt informerat samtycke till koloskopiprocedurerna och behandlingen i enlighet med Helsingforsdeklarationen.
Författarbidrag
ZC initierade utredningens koncept och design, förvärv, analys och tolkning av data, utarbetande och revidering av manuskriptet. KB deltog i insamling, analys och tolkning av data samt kritisk granskning av manuskriptet.
Intressekonfliktförklaring
Författarna förklarar att forskningen utfördes i avsaknad av kommersiella eller ekonomiska relationer som skulle kunna tolkas som en potentiell intressekonflikt.
Acknowledgments
Vi tackar Douglas Nelson MD, Robert Ganz MD, John Allen MD, David Lieberman MD, Douglas Rex MD, Linda Rabeneck MD, Aasma Shaukat MD, Zong-ming Eric Chen MD PhD, Jeffrey Rank MD, Joshua Colton MD och Cecil Chally MD för kritisk granskning och användbara förslag, Zengri Wang och Yongquan Xue PhD för hjälp med statistisk analys, Brian Hardwig för hjälp med att installera videoinspelning, Carlie Leyde, Amy Lounsbury, Martha Carland, JaNelle Gorg, Siri McCord, Karen Lang och Marit Brock för administrativt stöd. Vi tackar också Minnesota Gastroenterology endoskopisjuksköterskor för EMS-polypektomiassistans.
En poster med preliminära resultat av denna undersökning presenterades vid 2017 DDW i Chicago, USA. Ett abstract av postern publicerades i Gastrointestinal Endoscopy 2017; 85:AB520.
Supplementary Material
Supplementary Material for this article can be found online at: https://www.frontiersin.org/articles/10.3389/fmed.2018.00312/full#supplementary-material
Abkortningar
EMS, endoskopisk mukosal stripping; EMR, endoskopisk mukosal resektion; ESD, endoskopisk submucosal dissektion; TCSP, traditionell cold snare polypektomi; TA, tubulärt adenom; TVA(HD), tubulovillöst adenom (med höggradig dysplasi); SSA(CD), sessilt serrerat adenom (med cytologisk dysplasi); UC, ulcerös kolit.
1. Winawer SJ, Zauber AG, Ho MN, O’Brien MJ, Gottlieb LS, Sternberg SS, et al. Förebyggande av kolorektal cancer genom koloskopisk polypektomi. Den nationella arbetsgruppen för polypstudier. N Engl J Med. (1993) 329:1977-81. doi: 10.1056/NEJM19931212303292701
PubMed Abstract | CrossRef Full Text | Google Scholar
2. Zauber AG, Winawer SJ, O’Brien MJ, Lansdorp-Vogelaar I, van Ballegooijen M, Hankey BF, et al. Colonoscopic polypectomy and long-term prevention of colorectal-cancer deaths. N Engl J Med. (2012) 366:687-96. doi: 10.1056/NEJMoa1100370
PubMed Abstract | CrossRef Full Text | Google Scholar
3. Nishihara R, Wu K, Lochhead P, Morikawa T, Liao X, Qian ZR, et al. Long-term colorectal-cancer incidence and mortality after lower endoscopy. N Engl J Med. (2013) 369:1095-105. doi: 10.1056/NEJMoa1301969
PubMed Abstract | CrossRef Full Text | Google Scholar
4. Amri R, Bordeianou LG, Sylla P, Berger DL. Effekten av screeningkoloskopi på utfallet vid koloncancerkirurgi. JAMA Surg. (2013) 148:747-54. doi: 10.1001/jamasurg.2013.8
PubMed Abstract | CrossRef Full Text | Google Scholar
5. Brenner H, Stock C, Hoffmeister M. Effect of screening sigmoidoscopy and screening colonoscopy on colorectal cancer incidence and mortality: systematic review and meta-analysis of randomised controlled trials and observationsstudier. BMJ (2014) 348:g2467-78. doi: 10.1136/bmj.g2467
PubMed Abstract | CrossRef Full Text | Google Scholar
6. Sonnenberg A, Delcò F, Inadomi JM. Kostnadseffektivitet för koloskopi vid screening för kolorektalcancer. Ann Intern Med. (2000) 133:573-84. doi: 10.7326/0003-4819-133-8-200010170-00007
PubMed Abstract | CrossRef Full Text | Google Scholar
7. Lansdorp-Vogelaar I, Knudsen AB, Brenner H. Cost-effectiveness of colorectal cancer screening. Epidemiol Rev. (2011) 33:88-100. doi: 10.1093/epirev/mxr004
PubMed Abstract | CrossRef Full Text | Google Scholar
8. Lieberman DA Screening för kolorektalcancer hos personer med genomsnittlig risk: nuvarande metoder och nya frågor. JAMA Intern Med. (2014) 174:10-11. doi: 10.1001/jamainternmed.2013.11499
PubMed Abstract | CrossRef Full Text | Google Scholar
9. Barclay RL, Vicari JJ, Doughty AS, Johanson JF, Greenlaw RL. Colonoscopic withdrawal times and adenoma detection during screening colonoscopy. N Engl J Med. (2006) 355:2533-41. doi: 10.1056/NEJMoa055498
PubMed Abstract | CrossRef Full Text | Google Scholar
10. Kaminski MF, Regula J, Kraszewska E, Polkowski M, Wojciechowska U, Didkowska J, et al. Kvalitetsindikatorer för koloskopi och risken för intervallcancer. N Engl J Med. (2010) 362:1795-803. doi: 10.1056/NEJMoa0907667
PubMed Abstract | CrossRef Full Text | Google Scholar
11. Corley DA, Jensen CD, Marks AR, Zhao WK, Lee JK, Doubeni CA, et al. Adenomdetekteringsfrekvens och risk för kolorektal cancer och död. N Engl J Med. (2014) 370:1298-306. doi: 10.1056/NEJMoa1309086
CrossRef Full Text | Google Scholar
12. van Rijn JC, Reitsma JB, Stoker J, Bossuyt PM, van Deventer SJ, Dekker E. Polyp miss rate determined by tandem colonoscopy: a systematic review. Am J Gastroenterol. (2006) 101:343-50. doi: 10.1111/j.1572-0241.2006.00390.x
CrossRef Full Text | Google Scholar
13. Lieberman DA, Rex DK, Winawer SJ, Giardiello FM, Johnson DA, Levin TR. Guidelines for colonoscopy surveillance after screening and polypectomy: a consensus update by the US multi-society task force on colorectal cancer. Gastroenterology (2012) 143:844-57. doi: 10.1053/j.gastro.2012.06.001
PubMed Abstract | CrossRef Full Text | Google Scholar
14. Rex DK, Schoenfeld PS, Cohen J, Pike IM, Adler DG, Fennerty MB, et al. Kvalitetsindikatorer för koloskopi. Gastrointest Endosc. (2015) 81:31-53. doi: 10.1016/j.gie.2014.07.058
PubMed Abstract | CrossRef Full Text | Google Scholar
15. Waye JD, Lewis BS, Yessayan S. Colonoscopy: a prospective report of complications. J Clin Gastroenterol. (1992) 15:347-51. doi: 10.1097/00004836-199212000-00018
PubMed Abstract | CrossRef Full Text | Google Scholar
16. Ko CW, Dominitz JA. Komplikationer vid koloskopi: omfattning och hantering. Gastrointest Endosc Clin N Am. (2010) 20:659-71. doi: 10.1016/j.giec.2010.07.005
PubMed Abstract | CrossRef Full Text | Google Scholar
17. ASGE Standards of Practice Committee, Fisher, DA, Maple, JT, Ben-Menachem, T, Cash, BD, Decker, GA, et al. Komplikationer vid koloskopi. Gastrointest Endosc. (2011) 74:745-52. doi: 10.1016/j.gie.2011.07.025
CrossRef Full Text | Google Scholar
18. Pohl H, Srivastava A, Bensen SP, Anderson P, Rothstein RI, Gordon SR, et al. Incomplete polyp resection during colonoscopy-results of the complete adenoma resection (CARE) study. Gastroenterology (2013) 144:74-80. doi: 10.1053/j.gastro.2012.09.043
PubMed Abstract | CrossRef Full Text | Google Scholar
19. Adler J, Robertson DJ. Intervall kolorektal cancer efter koloskopi: utforskande av förklaringar och lösningar. Am J Gastroenterol. (2015) 110:1657-64. doi: 10.1038/ajg.2015.365
PubMed Abstract | CrossRef Full Text | Google Scholar
20. Ranasinghe I, Parzynski CS, Searfoss R, Montague J, Lin Z, Allen J, et al. Differences in colonoscopy quality among facilities: development of a post-colonoscopy risk-standardized rate of unplanned hospital visits. Gastroenterology (2016) 150:103-13. doi: 10.1053/j.gastro.2015.09.009
PubMed Abstract | CrossRef Full Text | Google Scholar
21. Rosen L, Bub DS, Reed JF, Nastasee SA. Blödning efter koloskopisk polypektomi. Dis Colon Rectum. (1993) 36:1126-31. doi: 10.1007/BF02052261
PubMed Abstract | CrossRef Full Text | Google Scholar
22. Gibbs DH, Opelka FG, Beck DE, Hicks TC, Timmcke AE, Gathright JB. Kolonblödning efter polypektomi. Dis Colon Rectum. (1996) 39:806-10. doi: 10.1007/BF02054448
PubMed Abstract | CrossRef Full Text | Google Scholar
23. Sorbi D, Norton I, Conio M, Balm R, Zinsmeister A, Gostout CJ. Blödning efter polypektomi i den nedre delen av GI: deskriptiv analys. Gastrointest Endosc. (2000) 51:690-6. doi: 10.1067/mge.2000.105773
PubMed Abstract | CrossRef Full Text | Google Scholar
24. Levin TR, Zhao W, Conell C, Seeff LC, Manninen DL, Shapiro JA, et al. Komplikationer vid koloskopi i ett integrerat hälsovårdssystem. Ann Intern Med. (2006) 145:880-6. doi: 10.7326/0003-4819-145-12-200612190-00004
PubMed Abstract | CrossRef Full Text | Google Scholar
25. Tolliver KA, Rex DK. Koloskopisk polypektomi. Gastroenterol Clin North Am. (2008) 37:229-51, ix. doi: 10.1016/j.gtc.2007.12.009
PubMed Abstract | CrossRef Full Text | Google Scholar
26. Rabeneck L, Paszat LF, Hilsden RJ, Saskin R, Leddin D, Grunfeld E, et al. Blödning och perforation efter poliklinisk koloskopi och deras riskfaktorer i vanlig klinisk praxis. Gastroenterology (2008) 135:1899-906. doi: 10.1053/j.gastro.2008.08.058
PubMed Abstract | CrossRef Full Text | Google Scholar
27. Warren JL, Klabunde CN, Mariotto AB, Meekins A, Topor M, Brown ML, et al. Biverkningar efter koloskopi i öppenvården i Medicare-populationen. Ann Intern Med. (2009) 150:849-57. doi: 10.7326/0003-4819-150-12-200906160-00008
PubMed Abstract | CrossRef Full Text | Google Scholar
28. Sawhney MS, Salfiti N, Nelson DB, Lederle FA, Bond JH. Riskfaktorer för allvarlig försenad blödning efter polypektomi. Endoscopy (2008) 40:115-9. doi: 10.1055/s-2007-966959
PubMed Abstract | CrossRef Full Text | Google Scholar
29. Metz AJ, Bourke MJ, Moss A, Williams SJ, Swan MP, Byth K. Faktorer som förutsäger blödning efter endoskopisk mukosalresektion av stora kolonlesioner. Endoscopy (2011) 43:506-11. doi: 10.1055/s-0030-1256346
PubMed Abstract | CrossRef Full Text | Google Scholar
30. Bahin FF, Rasouli KN, Byth K, Hourigan LF, Singh R, Brown GJ, et al. Prediction of clinical significant bleeding following wide-field endoscopic resection of large sessile and laterally spreading colorectal lesions: a clinical risk score. Am J Gastroenterol. (2016) 111:1115-22. doi: 10.1038/ajg.2016.235
PubMed Abstract | CrossRef Full Text | Google Scholar
31. Albéniz E, Fraile M, Ibáñez B, Alonso-Aguirre P, Martínez-Ares D, Soto S, et al. A scoring system to determine risk of delayed bleeding after endoscopic mucosal resection of large colorectal lesions. Clin Gastroenterol Hepatol. (2016) 14:1140-7. doi: 10.1016/j.cgh.2016.03.021
PubMed Abstract | CrossRef Full Text | Google Scholar
32. Wolff WI, Shinya H. Tidig diagnos av cancer i tjocktarmen genom kolonendoskopi (koloskopi). Cancer (1974) 34:912-34.
Google Scholar
33. Tedesco FJ. Koloskopisk polypektomi. In: Silvia SE, editor. Therapeutic Gastrointestinal Endoscopy (1984) New York, NY: Igaku-Shoin. s. 269-88.
Google Scholar
34. Waye JD. Polypektomi – grundläggande principer. In: Waye JD, Rex DK, Williams CB, red. Colonoscopy Principles and Practice. Malden, MA; Oxford: Carlton (2003) s. 410-9. doi: 10.1002/9780470986943.ch35
CrossRef Full Text | Google Scholar
35. Waye JD. Polypektomi: grundläggande principer. In: Waye JD, Rex DK, Williams CB, red. Colonoscopy Principles and Practice. Oxford; Hoboken, NJ: Wiley-Blackwell (2009) s. 572-81.
Google Scholar
36. Meeroff JC. Avlägsnande av medelstora fastsittande polyper i tjocktarmen utan diatermi. Gastrointest Endosc. (1989) 35:136. doi: 10.1016/S0016-5107(89)72740-1
PubMed Abstract | CrossRef Full Text | Google Scholar
37. Tappero G, Gaia E, De Giuli P, Martini S, Gubetta L, Emanuelli G. Cold snare excision of small colorectal polyps. Gastrointest Endosc. (1992) 38:310-3. doi: 10.1016/S0016-5107(92)70422-2
PubMed Abstract | CrossRef Full Text | Google Scholar
38. Chen ZJ., Batts K. P. (2017). Mo2011 eliminering av blödning efter polypektomi och mer komplett polypborttagning med endoskopisk mucosal stripping (EMS). Gastroenterol. Endos. 85(Suppl. 5):AB520. Abstract Mo2011. doi: 10.1016/j.gie.2017.03.1198
CrossRef Full Text | Google Scholar
39. Horiuchi A, Nakayama Y, Kajiyama M, Tanaka N, Sano K, Graham DY. Borttagning av små kolorektala polyper hos antikoagulerade patienter: en prospektiv randomiserad jämförelse av cold snare och konventionell polypektomi. Gastrointest Endosc. (2014) 79:417-23. doi: 10.1016/j.gie.2013.08.040
PubMed Abstract | CrossRef Full Text | Google Scholar
40. Zhang Q, Gao P, Han B, Xu J, Shen Y. Polypektomi för fullständig endoskopisk resektion av små kolorektala polyper. Gastrointest Endosc. (2017). 87(3):733-740. doi: 10.1016/j.gie.2017.06.010
PubMed Abstract | CrossRef Full Text | Google Scholar
41. Paspatis GA, Tribonias G, Konstantinidis K, Theodoropoulou A, Vardas E, Voudoukis E, et al. A prospective randomized comparison of cold vs hot snare polypectomy in the occurrence of postpolypectomy bleeding in small colonic polyps. Colorectal Dis. (2011) 13:e345-8. doi: 10.1111/j.1463-1318.2011.02696.x
PubMed Abstract | CrossRef Full Text | Google Scholar
42. Repici A, Hassan C, Vitetta E, Ferrara E, Manes G, Gullotti G, et al. Safety of cold polypectomy for < 10mm polyps at colonoscopy: a prospective multicenter study. Endoskopi. (2012) 44:27-31. doi: 10.1055/s-0031-1291387
PubMed Abstract | CrossRef Full Text | Google Scholar
43. Tutticci N, Burgess NG, Pellise M, Mcleod D, Bourke MJ. Karaktärisering och betydelse av protrusioner i slemhinnedefekten efter cold snare-polypektomi. Gastrointest Endosc. (2015) 82:523-8. doi: 10.1016/j.gie.2015.01.051
PubMed Abstract | CrossRef Full Text | Google Scholar