US Pharm. 2008;33(3)(OTC suppl):4-7.
Astma är en lungsjukdom som kännetecknas av reversibel luftflödesobstruktion och bronkial hyperreaktivitet. Det centrala kännetecknet för astma är inflammation, vilket leder till återkommande episoder av väsande andning, hosta, andnöd och trånghet i bröstet.1,2 Målet med behandlingen är att få kontroll över sjukdomen för att bibehålla en normal livskvalitet.
Bördan av astma har stadigt ökat under de senaste tre decennierna. År 1970 hade cirka 3 % av befolkningen astma, jämfört med 5,5 % och 7,7 % 1995 respektive 2005.3 Den sistnämnda uppskattningen motsvarar cirka 22,2 miljoner amerikaner.2,3 I och med att prevalensen av denna sjukdom ökar i USA ökar också morbiditeten och mortaliteten på grund av astma. År 2004 var astma orsaken till 1,8 miljoner besök på akutmottagningen, 497 000 sjukhusinläggningar och 4 055 dödsfall.3
Behandling baserad på astmakontroll
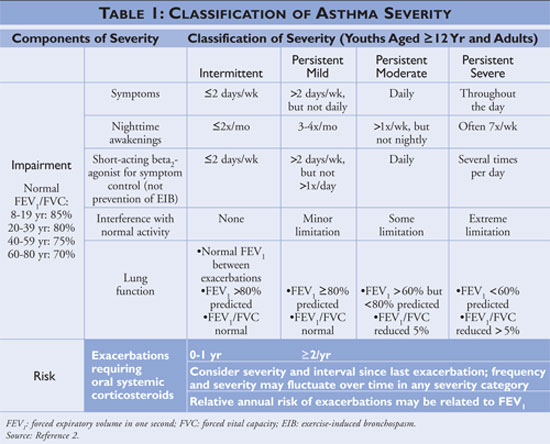
National Asthma Education and Prevention Program (NAEPP), en avdelning av National Heart, Lung, and Blood Institute, publicerar Guidelines for the Diagnosis and Management of Asthma (riktlinjer för diagnostisering och behandling av astma), som senast uppdaterades 2007.2 Riktlinjerna klassificerar astmas allvarlighetsgrad som intermittent eller ihållande baserat på symtom och frekvensen av användning av snabbverkande mediciner. Personer med intermittent astma har sällan symtom, använder följaktligen sällan snabbverkande läkemedel och stör inte den normala aktiviteten. Om astman är mindre kontrollerad klassificeras astmans svårighetsgrad som persisterande (se TABELL 1).
Riktlinjerna beskriver hörnstenarna i astmahanteringen som utbildning i självförvaltning, användning av snabbverkande mediciner och användning av mediciner för långtidskontroll hos personer med persisterande astma. Hälso- och sjukvårdspersonal som erbjuder utbildning i självhantering bör instruera patienterna att identifiera och undvika astmautlösare när det är möjligt, använda farmakologiska terapier på rätt sätt och utarbeta en astmahandlingsplan. Snabbt avtagande läkemedel bör sättas in för alla patienter med astmadiagnos och kan användas som monoterapi hos personer med intermittent astma. Personer med diagnosen persisterande astma bör dock få ett eller flera långtidskontrollmediciner till sin behandling. Långsiktiga kontrollmediciner inkluderar inhalerade kortikosteroider, leukotrienmodifierare, långverkande beta-agonister och teofyllin (se TABELL 2).

Riktlinjerna noterar också att cirka 30 % av den amerikanska befolkningen använder sig av komplementära och alternativa mediciner och interventioner. För närvarande finns det dock inte tillräckliga bevis för att rekommendera dessa behandlingsmetoder för astma. Riktlinjerna avråder från användning av naturläkemedel för behandling av astma på grund av bristen på säkerhets- och effektdata.
Fri receptfria astmaprodukter och deras reglering
Fri receptfria astmaprodukter har funnits tillgängliga sedan 1950-talet, även om en del av de aktiva beståndsdelarna har förändrats avsevärt under årens lopp. För närvarande tillgängliga receptfria aktiva ingredienser är efedrin – med eller utan guaifenesin – och adrenalin. Teofyllin och fenobarbital har tidigare varit aktiva ingredienser i receptfria astmamediciner, men båda klassificeras nu som receptbelagda produkter.4
Under de senaste tre decennierna har FDA vidtagit åtgärder när det gäller regleringen av receptfria behandlingar för astma. År 1976 drog FDA slutsatsen att inhalerat adrenalin gav snabb och effektiv lindring vid mild till måttlig astma. År 1982 drog FDA återigen slutsatsen i en preliminär slutlig monografi: ”Epinefrin, epinefrinbitartrat och epinefrinhydroklorid (racemiskt; har sedan dess bytt namn till racepinefrinhydroklorid) i trycksatta doseringsformer för inhalationsaerosol kan allmänt erkännas som säkra och effektiva för receptfri användning i en dosering för vuxna och barn från 4 år och uppåt på 1 till 2 inhalationer av en doserad dos som motsvarar 0,5 %.16 till 0,25 mg epinefrin per inhalation inte oftare än var tredje timme. ”5,6
År 1986 granskade FDA efedrinprodukter för bronkdilatation och godkände denna aktiva ingrediens som allmänt erkänd som säker och effektiv för receptfri användning. Det året beslutade FDA att uppgifterna var otillräckliga för att begränsa inhalerad epinefrin till receptbelagd användning och att fördelarna med receptfri tillgänglighet övervägde riskerna. FDA drog slutsatsen att en utökad och reviderad märkning skulle gynna konsumenterna.5,6
Efter rapporter om livshotande händelser och dödsfall som kan tillskrivas receptfria kombinationsprodukter som innehåller teofyllin, utfärdade FDA 1995 ett slutgiltigt beslut om att dessa produkter inte var säkra eller effektiva.7 Produkter som innehöll en kombination av efedrin och teofyllin lades därför ned och en del av dem omformulerades till att innehålla efedrin och guaifenesin. FDA föreslog också 1995 att efedrin skulle avlägsnas från den receptfria marknaden på grund av dess roll i tillverkningen av metamfetamin och methcathinon och dess missbruk för viktkontroll och muskelförstärkning.7
Under 1996 ändrade FDA den slutliga monografin från 1986 för att ta bort monografistatusen för receptfria bronkdilatatorer.6 I stället måste tillverkare av nya receptfria dosinhalatorer lämna in en godkänd ansökan som innehåller information som inte finns i monografin.6 För närvarande marknadsförda receptfria bronkdilatatorer påverkades inte av denna ändring.
Trots FDA:s förslag att avlägsna efedrin från den receptfria marknaden på grund av dess användning som grundämne vid metamfetamintillverkning, finns produkten fortfarande tillgänglig som receptfritt läkemedel. I stället gav Combat Methamphetamine Epidemic Act från 2005, som införlivades i Patriot Act 2006, status som receptfria produkter som innehåller efedrin bakom disk på recept.8 Konsumenter som vill köpa produkter som innehåller efedrin måste nu visa upp ett statligt utfärdat foto-ID på ett apotek, eftersom dessa produkter inte längre säljs lagligt i närbutiker eller lagerbutiker utan ett registrerat apotek.
Som en del av det globala folkhälsoskyddet bildades ett internationellt avtal för att minska och så småningom eliminera produkter som innehåller ozonnedbrytande ämnen (ODS), som t.ex. klorfluorkarboner (CFC) som finns i inhalationsapparater med doseringsutrustning (MDI). Avtalet gav upphov till 1987 års Montrealprotokoll och därefter 1990 års ändringar av Clean Air Act.9-11 Avtalet ger ett undantag för användning av klorfluorkarboner i inhalationsaerosoler som används för astmabehandling om FDA anser att produkten är nödvändig.12 Astmamediciner som inte är receptbelagda har förblivit under beteckningen ”nödvändig användning”. År 2007 tillkännagav FDA dock ett förslag om att ta bort beteckningen ”viktig användning” för inhalerad adrenalin från och med den 31 december 2010.13 FDA använde följande kriterier, som återfinns i 21 CFR 2.125(g)(2), för att se över beteckningen ”viktig användning” för inhalerad adrenalin: ”(i): Det finns betydande tekniska hinder för att formulera produkten utan ozonnedbrytande ämnen, (ii): Produkten kommer att ge en otillgänglig viktig nytta för folkhälsan, och (iii): Användningen av produkten släpper inte ut kumulativt betydande mängder ozonnedbrytande ämnen i atmosfären eller så är utsläppet motiverat med tanke på den otillgängliga viktiga nyttan för folkhälsan. ”13 Livsmedelsverket tar för närvarande emot kommentarer i denna fråga innan det slutgiltiga beslutet fattas.
Säkerhet och effekt av receptfria produkter
Som framgår av de olika förslag som lagts fram och åtgärder som FDA vidtagit när det gäller astmaprodukters receptfria status, har det under de senaste decennierna förts en omfattande debatt om säkerheten och effekten av de aktiva ingredienserna i dessa produkter. Även om dessa produkter inte marknadsförs aktivt innebär deras tillgänglighet att deras säkerhet och effektivitet är av avgörande betydelse för konsumenterna.
Efedrin: Efedrinprodukter med en enda ingrediens som används som bronkdilaterande medel har av FDA sedan 1986 betraktats som allmänt erkända som säkra och effektiva.14 Efedrin frigör epinefrin från vävnader, vilket utlöser alfa-adrenerga och icke-selektiva beta-adrenerga receptoraktivitet. Efedrins effektivitet för bronkdilatation har visats i studier från 1950-talet. Egenskaper som gör efedrin mindre önskvärt som bronkdilaterare är bland annat en långsammare verkan än inhalerade produkter (15 minuter till en timme) och icke-selektivitet för betastimulering, vilket skulle kunna bidra till kardiovaskulära biverkningar.15-17 Studier har dock visat motstridiga resultat när det gäller kardiovaskulära biverkningar som kan tillskrivas efedrinanvändning vid märkta doser på 12,5 till 25 mg.16
Epinefrin: Epinefrin: Epinefrin uppvisar samma alfa- och beta-adrenerga receptoraktivitet som efedrin; därför finns samma farhågor när det gäller risken för kardiovaskulära biverkningar. Inhalerat adrenalin har en mycket snabbare verkan (15 sekunder) än oralt efedrin, vilket gör det till ett lämpligare val för omedelbar lindring av en akut astmaexacerbation.6 Dess korta verkningstid (23 minuter) kan dock göra det nödvändigt för patienten att använda produkten upprepade gånger för fortsatt lindring i stället för att följa märkningsanvisningarna om högst två inhalationer inom tre timmar.6 Receptfria adrenalininhalatorer verkar vara säkra och effektiva för patienter med mild, intermittent astma när de används enligt märkningen.5 Detta är dock fortfarande en källa till kontroverser, eftersom många vårdgivare är oroliga för att patienter som förlitar sig på receptfria inhalatorer kanske inte får lämplig sjukdomsbehandling av ett vårdteam, vilket kan leda till allvarliga återverkningar.
Guaifenesin: Guaifenesin används i kombination med efedrin för astmabehandling och erkänns som säkert och effektivt när produkten är märkt för hosta i samband med astma.14 Även om guaifenesin är ett FDA-godkänt slemlösande medel har det inga bronkdilaterande effekter. Därför bidrar det inte med någon ytterligare fördel till efedrinprodukten vid en akut exacerbation.17
Användning av receptfria astmaprodukter
En undersökning som Wyeth Consumer Healthcare (WCH) genomförde 1999 visade att ungefär sex miljoner (30 %) personer med astma använder epinefrininhalatorer.6 Respondenternas självrapportering tyder på att ungefär 20 % av dessa sex miljoner skulle klassificeras som personer med mild till måttlig ihållande astma, vilket inte ingår i den märkta användningen av denna produkt.5 Riktlinjerna från NAEPP främjar användningen av kortverkande beta-agonister åtminstone vid behov av alla personer som lider av astma; riktlinjerna nämner dock inte specifikt inhalerad epinefrin som ett behandlingsalternativ.
Under 2005 genomförde WCH en Internetundersökning med 330 personer om användningen av receptfria bronkdilatatorer för behandling av deras symtom. WCH konstaterade att 92 % av de som använde receptfria bronkdilatatorer hade diagnostiserats med astma, 91 % använde inhalerad adrenalin endast vid en akut astmaexacerbation, 31 % hade ingen sjukvårdsförsäkring och 38 % hade ingen receptbelagd försäkring.6 WCH extrapolerade dessa resultat för att uppskatta att cirka 5 % till 10 % av alla astmatiker använder receptfria bronkdilatatorer som monoterapi.6 De främsta anledningarna till receptfri användning – enkel tillgång och lägre kostnad – korrelerar direkt med vårdpersonalens oro för att personer som använder receptfria astmaprodukter kanske inte får lämplig sjukdomsbehandling.6
Diskussion
De egenskaper som är önskvärda vid akut astmabehandling är bland annat effektivitet som bronkdilaterare, säkerhet när de tas enligt märkningen, snabb verkningsstart och lång verkningstid. Både inhalerat adrenalin och oralt efedrin har visat sig vara effektiva i prövningar i årtionden. Med tanke på de blandade kardiovaskulära resultaten i kliniska prövningar är säkerheten vid användning av receptfria bronkdilatatorer av personer som kanske inte följs medicinskt en viktig fråga för vårdgivarna. Inhalerat adrenalin har en snabbare verkan än oralt efedrin, men dess korta verkningstid kan begränsa dess effektivitet.
Tillgången till oralt efedrin har sedan 2006 begränsats av dess status som receptfritt läkemedel. Tillgängligheten av inhalerad epinefrin beror på FDA:s beslut om huruvida denna formulering kommer att behålla sin beteckning som viktig för användning. Det finns inga receptfria alternativ till de CFC-haltiga bronkdilatatorer som för närvarande marknadsförs och som inte är receptbelagda.12 En tillverkare försökte omformulera sin receptfria inhalerade adrenalinprodukt med ett drivmedel av hydrofluoroalkan, med oönskade effekter för användaren. Företaget har samarbetat med ett annat läkemedelsföretag för att omformulera produkten i avvaktan på att kunna lämna in en ansökan till FDA senast 2011.6 Viktiga problem när det gäller alternativa drivmedel är bland annat att det behövs en effektiv tillförsel av adrenalin och att det finns data om säkerhet och effekt för den nya produkten till följd av förändringarna.18
I samband med att FDA beslutar om huruvida man ska avskaffa beteckningen för viktiga användningsområden för inhalerad adrenalin undersöker FDA inte säkerheten eller effektiviteten hos de CFC-haltiga produkter som för närvarande saluförs, utan snarare hur folkhälsan påverkas om beteckningen avskaffas. I brev från National Association of Chain Drug Stores och American Pharmacists Association till FDA om förslaget att avskaffa beteckningen ”essentiell användning” var den främsta oron den potentiella negativa effekten på nuvarande användare av receptfria inhalatorer om produkterna skulle bli otillgängliga.19,20 FDA har förklarat att om den föreslagna regeln om att avskaffa beteckningen ”essentiell användning” blir slutgiltig och det inte finns några receptfria alternativ, kommer det att bli nödvändigt för konsumenterna att skaffa sig ett recept för en alternativ produkt.12 Många konsumenter som använder inhalerad adrenalin kan välja att avstå från astmabehandling eller söka alternativ receptfri behandling.
Det är absolut nödvändigt att läkarkåren gör allmänheten medveten om allvaret i konsekvenserna av okontrollerad astma och att varje person som upplever andningssvårigheter bör uppsöka en vårdgivare för diagnos och behandling. En patient som väljer att använda receptfria bronkdilatatorer bör uppmanas att informera sin vårdgivare; patienten bör också få råd om skillnaden i märkningsanvisningar mellan receptfria och receptbelagda inhalatorer. Den nuvarande fortsatta tillgängligheten av receptfria bronkdilatatorer kräver informerad rådgivning till patienterna för att förhindra felaktig användning av dessa produkter och efterföljande biverkningar.
1. Moorman JE, Rudd RS, Johnson CA, et al. National Surveillance for Asthma–United States, 1980-2004. MMWR. Oct 19, 2007;56:1-14, 18-54.
2. Expertpanelrapport 3: Riktlinjer för diagnos och behandling av astma. Nationellt program för utbildning och förebyggande av astma. Bethesda, MD: National Heart, Lung, and Blood Institute, National Institutes of Health; 2007.
3. Akinbami L. Astmaprevalens, vårdanvändning och dödlighet: USA, 2003-05. National Center for Health Statistics. www.cdc.gov/nchs/products/pubs
/pubd/hestats/ashtma03-05/asthma03-05.htm. Tillgänglig den 10 december 2007.
4. W. Steven Pray. OTCprodukter och astmabehandling. US Pharm. 1997;22(7):18-22.
5. Dickinson BD, Altman RD, Deitchman SD, Champion HC. Safety of over-the-counter inhalators for asthma: report of the Council on Scientific Affairs. Chest. 2000;118:522-526.
6. Wyeth ConsumerHealthcare. 2005N-0374. Användning av ozonnedbrytande ämnen: fastställande av nödvändig användning av receptfria dosinhalatorer med epinefrin. Informationsdokument. Den 19 december 2005. www.fda.gov/ohrms/dockets/ac
/06/briefing/2006-4200B1_01_01-Wyeth-Backgrounder.pdf. Tillgänglig den 30 december 2007.
7. Kupec IF. Teofyllinhaltiga bronkdilatatorer och efedrinläkemedel. Svar T95-40. 27 juli 1995. www.fda.gov/bbs/topics/ANSWERS/ANS00675.html. Tillgänglig den 10 december 2007.
8. Drug Enforcement Administration. Allmän information om Combat Methamphetamine Epidemic Act of 2005 . Maj 2006. www.deadiversion.usdoj.gov/meth/cma2005_general_info.pdf. Tillgänglig den 4 februari 2008.
9. Jarabek AM, Fisher JW, Rubenstein R, et al. Mechanistic insights help the search for CFC substitutes: risk assessment of HCFC-123 as an example. Risk Anal. 1994;14:231-250.
10. DeCanio SJ, Norman CS. Ekonomi för ”undantag för viktiga användningsområden” för dosinhalatorer enligt Montrealprotokollet. J Environ Manage.2007;85:1-8.
11. D’Souza S. Montrealprotokollet och undantag för viktiga användningsområden. J Aerosol Med. 1995;8(suppl 1):S13-S17.
12. Food and Drug Administration (livsmedels- och läkemedelsmyndigheten). FDA News. FDA föreslår utfasning av CFC i dosinhalatorer för adrenalin. www.fda.gov/bbs/topics/NEWS
/2007/NEW01706.html. Tillgänglig den 10 december 2007.
13. Food and Drug Administration. Code of Federal Regulation 21 CFR part 2 2007N-0262. www.fda.gov/ohrms/dockets/98fr/cd0612.pdf. Tillgänglig den 6 februari 2008.
14. Whitehall-Robins. RE: docket no. 98N-0148; Fed. Reg. 13258, International Drug Scheduling; Convention on Psychotropic Substances. Den 16 april 1998. www.fda.gov/ohrms/dockets/dockets/98n0148/c000010.pdf. Tillgänglig den 30 december 2007.
15. Lexi-Comp Online. www.crlonline.com. Tillgänglig den 28 december 2007.
16. Tashkin DP, Meth R, Simmons DH, Lee YE. Dubbelblind jämförelse av akuta bronkiella och kardiovaskulära effekter av oralt terbutalin och efedrin. Chest. 1975;68:155-161.
17. Dulfano MJ. De nya orala bronkodilatorerna . Chest.1975;68:133-134.
18. Förkylnings-, host-, allergi-, bronkdilaterande och antiastmatiska läkemedel för receptfritt bruk hos människor; ändring av monografi för receptfria bronkdilaterande läkemedel. Fed Regist. 1996; 61:25142-25147.
19. National Association of Chain Drug Stores. Angående: Användning av ozonnedbrytande drivmedel; borttagande av beteckningen ”viktig användning” för receptfria dosinhalatorer med epinefrin. 6 januari 2006. www.fda.gov/ohrms/dockets/dockets/05n0374/05n-0374-EC6-Attach-1.pdf. Tillgänglig den 6 februari 2008.
20. Uttalande från American Pharmacists Association (APhA) till Food and Drug Administration’s Nonprescription Drugs Advisory Committee och Pulmonary-Allergy Drugs Advisory Committee. Användning av ozonnedbrytande ämnen: fastställande av nödvändig användning av receptfria dosinhalatorer för epinefrin. 24 januari 2006. www.fda.gov/ohrms/dockets/dockets/05n0374/05N-0374-EC10-Attach-1.pdf. Tillgänglig den 6 februari 2008.
Om du vill kommentera denna artikel, kontakta [email protected].