Termi brachydaktylia käsittää ryhmän luun dysplasioita, jotka koskevat käsien ja jalkaterien falangia- ja/tai metakarpaali- ja metatarsaaliluuta. Niitä on 5 tyyppiä (A-E) ja useita alatyyppejä (A1-A4; E1-E3). Kyseessä on autosomaalinen dominantti periytymismalli, jonka penetranssi on vaihteleva. Tapaukset, joissa periytyminen on resessiivistä, ovat erittäin harvinaisia.
C-tyypin brakydaktylylle (BDC) on ominaista toisen, kolmannen ja viidennen sormen keskimmäisten falangien sekä ensimmäisen metakarpaaliluun lyheneminen, ja siihen voi liittyä myös etusormen ulnaarinen poikkeama, polydaktylia tai toisen ja kolmannen sormen proksimaalisten tai keskimmäisten falangien selvä hypersegmentaatio. Neljäs sormi on vähiten vaurioitunut ja yleensä pisin.1-3 ”Enkelinmuotoiset” falangit (kuva 1A) ovat tyypillisiä BDC:lle, mutta ne eivät ole patognomonisia, sillä niitä voi esiintyä myös enkelinmuotoisen falango-epifyysisen dysplasian nimellä tunnetussa häiriössä. On mahdollista, että tämä häiriö ja BDC kuuluvat samaan kliiniseen spektriin.1 BDC:ssä tämä piirre normalisoituu, kun käden luiden fyseaalinen sulkeutuminen on saatu päätökseen, ja se päättyy yksinkertaisena brachydaktyliana.1 Muita BDC:hen liittyviä poikkeavuuksia ovat lyhytkasvuisuus, johon liittyy viivästynyttä luun ikää, Madelungin epämuodostuma, lonkkanivelen toimintahäiriö, talipes valgus- tai equinovarus-poikkileikkaus tai keskimmäisten falangeiden puuttuminen varpaankärjistä.2,3,3
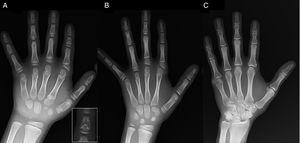
(A) Röntgenkuva koehenkilön vasemmasta kädestä (kronologinen ikä 7 vuotta; luuston ikä 5 vuotta), jossa näkyy anomaalisen ensimmäisen metakarpaalin (kaksinkertainen proksimaalinen ja distaalinen epifyysilevy) ja toisen, kolmannen ja viidennen sormen keskimmäisten falangien lyheneminen. Toisessa sormessa on ulnaarinen poikkeama, ja neljäs sormi on vähiten vaurioitunut ja pisin vasemmassa kädessä. Toisen ja kolmannen sormen proksimaaliset epifyysit ovat dysplastisia, ja toisessa sormessa on silmiinpistävä enkelinmuotoinen keskimmäinen falangi (sisäkuva A:ssa). (B). Röntgenkuva koehenkilön siskon vasemmasta kädestä (iältään 5½ vuotta, ei viivettä luun iässä), jossa toisen, kolmannen ja viidennen sormen keskimmäiset falangit ovat lyhentyneet ja neljäs sormi on normaali. Tässä tapauksessa ensimmäinen metakarpaali oli normaali. Merkittävin piirre on toisen sormen proksimaalisen falangin proksimaalisen epifyysin kolmion muoto, joka on samanlainen kuin veljellä, ja keskimmäisen sormen keskimmäisen falangin trapetsimainen muoto. Veljensä tavoin hänen toisessa sormessaan on ulnaarinen poikkeama. (C) Röntgenkuva koehenkilön isän vasemmasta kädestä, jossa näkyy vain luinen jäännös postaksiaalisesta heksadaktyaliasta, joka korjattiin kirurgisesti lapsuudessa.
Esittelemme tapauksen 7-vuotiaasta pojasta, jonka radiologiset piirteet sopivat BDC:hen ja joka lähetettiin arvioitavaksi lyhytkasvuisuudesta (z-arvo -1,8). Hänen isällään oli yksipuolinen postaksiaalinen polydaktylia, jota esiintyi myös isänpuoleisella sedällä molemminpuolisesti. Vasemman käden ja ranteen röntgentutkimuksessa todettiin, että luuston ikä oli 2 vuotta kronologista ikää nuorempi ja että luustossa oli poikkeavuuksia, jotka johtivat luustotutkimuksen tekemiseen. Tutkimuksessa havaittiin poikkeavuuksia käsissä (kuva 1A) ja hienovaraisia poikkeavuuksia jaloissa (lievä epifyysinen dysplasia joidenkin varpaiden proksimaalisissa falangioissa). Kuusivuotiaan sisaren radiologisessa arvioinnissa havaittiin kädessä samanlaisia vaurioita kuin koehenkilöllä, vaikkakin vähemmän selviä (kuva 1B). Isän kädestä otetussa röntgenkuvassa (kuva 1C) havaittiin vain luun jäänne postaksiaalisesta heksadaktyaliasta, joka oli kirurgisesti korjattu lapsuudessa.
Sekvensointi GDF5-geenistä koehenkilöllä paljasti heterotsygoottisen pistesubstituution eksonissa 2 (c.1462A>T), joka johti ennenaikaiseen stop-kodoniin (p.Lys488*, nonsense-mutaatio) ja typistettyyn proteiiniin, joka on 14 aminohappoa lyhyempi kuin villi proteiini (kuva 2A). Tämä mutaatio löytyi myös potilaan isältä ja sisarelta, mutta ei terveeltä äidiltä (kuva 2B). Kuvassa 2C esitetään perheen sukutaulu. Kyseessä on uusi variantti, joka on todennäköisesti patogeeninen ja jolla on autosomaalinen dominoiva periytymismalli.
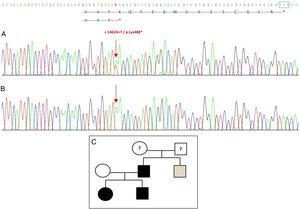
GDF5-geenissä havaittu uusi mutaatio. (A) Koehenkilön eksoni 2:n geenisekvenssi, jossa näkyy c.1462A>T-mutaatio, joka johtaa ennenaikaiseen stop-kodoniin ja typistettyyn proteiiniin (p.Lys488*) (olemme merkinneet stop-kodonin normaalin sijainnin vihreällä neliöllä). (B) Saman alueen normaali sekvenssi terveellä äidillä. (C) Perheen sukupuu: isällä ja molemmilla lapsilla (mustalla) on vahvistettu mutaatio GDF5:ssä. Terve äiti on merkitty valkoisella. Harmaa neliö edustaa isänpuoleista setää, jolla on molemminpuolinen postaksiaalinen polydaktylia ja jolla todennäköisesti on mutaatio.
Kasvun erilaistumistekijä 5 (Growth differentiation factor 5, GDF5) liittyy läheisesti luun morfogeneettisiin proteiineihin, ja se kuuluu transformoivaan kasvutekijä β:n superperheeseen, jonka avulla se osallistuu luuston ja nivelten kehitykseen alkiossa.4 GDF5-geeni on luuston epämuodostumiin liittyvien sairauksien mutaatiokeskittymä.5 Useimmat homotsygoottiset tai yhdistelmäheterotsygoottiset mutaatiot liittyvät vakaviin sairauksiin: Greben tyyppinen kondrodysplasia (OMIM 200700), Hunter-Thomsonin tyyppinen akromesomelinen dysplasia (OMIM 201250) tai Du Panin oireyhtymä (OMIM 228900). Toisaalta heterotsygoottiset mutaatiot liittyvät lievempiin luuston dysplasioihin: proksimaalinen symphalangismi 1 B (OMIM 615298) ja multippeli synostoosioireyhtymä tyyppi 2 (OMIM 610017), joihin molempiin liittyy missense-mutaatioita, jotka johtavat toiminnan vahvistumiseen, sekä brachydaktylia tyyppi A1 ja A2, joihin liittyy myös missense-mutaatioita, mutta jotka johtavat toiminnan häviämiseen.5 5 Brachydaktylia tyyppi C liittyy heterotsygoottisiin mutaatioihin, jotka aiheuttavat toimintakadon, vaikka on myös raportoitu kolme tapausta, joissa periytyminen on resessiivistä6. Useimmat BDC:hen liittyvät mutaatiot ovat frameshift-mutaatioita geenin prodomainin osassa, kun taas useimmat kypsän domainin mutaatiot ovat missense-mutaatioita, joiden fenotyyppinen ilmentyminen on hyvin vaihtelevaa.4
Tässä esittelemässämme perheessä on nonsense-mutaatio alueella, joka koodaa proteiinin aktiivista domeenia, mikä johtaa proteiinin 14 viimeisen aminohapon poistumiseen. Tämä on toinen kirjallisuudessa kuvattu aktiiviseen kypsään domeeniin vaikuttava nonsense-mutaatio.3 Ensimmäinen on samankaltainen mutaatio tässä kuvaamassamme perheessä mutatoitunutta aminohappoa välittömästi edeltävässä aminohapossa (p.Tyr487*/c.1461T>G), mikä viittaa siihen, että molemmat synnyttävät mutantteja monomeerejä ja GDF5:n funktionaalista haploinsuffisienssiä ja aiheuttavat siten BDC:tä.
Rahoitus
Tämä tutkimus rahoitettiin osittain hankkeilla PI13/00467 ja PI13/01295, jotka on integroitu Espanjan hallituksen 2013-2016 R&D&I-suunnitelmaan ja joita Instituto de Salud Carlos III:n (ISCIII) tutkimuksen arvioinnin ja edistämisen apulaispääosasto yhteisrahoitti, Euroopan aluekehitysrahasto (EAKR) ja Centro de Investigación Biomédica en Red sobre Fisiopatología de la Obesidad y la Nutrición (lihavuuden ja ravitsemuksen fysiopatologiaa käsittelevä biolääketieteellinen tutkimusverkostokeskus ), ISCIII, Madrid.